
分析 根据质量守恒定律可知,过程中质量的减少是因为生成了二氧化碳,所以可以求算二氧化碳的质量,根据二氧化碳和对应的化学方程式求算碳酸钠和HCl以及生成的氯化钠的质量,进而求算对应的质量分数.
解答 解:根据质量守恒定律可得,生成的二氧化碳的质量为11g+50g+64.4g-121g=4.4g
设参加反应的碳酸钠的质量为x,生成的氯化钠的质量为y,参加反应的HCl的质量为z
Na2CO3+2HCl═2NaCl+H2O+CO2↑
106 73 117 44
x z y 4.4g
$\frac{106}{x}$=$\frac{73}{z}$=$\frac{117}{y}$=$\frac{44}{4.4g}$
x=10.6g
y=11.7g
z=7.3g
该纯碱样品的纯度为$\frac{10.6g}{11g}$×100%≈96.4%.
所加稀盐酸中溶质的质量分数为$\frac{7.3g}{64.4g}$×100%≈11.3%.
所得溶液中溶质的质量分数为$\frac{11g-10.6g+11.7g}{121g}$×100%=10.0%.
答:(1)该纯碱样品的纯度约为96.4%;
(2)所加稀盐酸中溶质的质量分数约为11.3%;
(3)所得溶液中溶质的质量分数为10.0%.
点评 根据化学方程式计算时,第一要正确书写化学方程式,第二要使用正确的数据,第三计算过程要完整.


科目:初中化学 来源: 题型:填空题
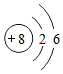 所示.
所示.
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
| 实验内容 | 实验现象 | 实验结论或解释 |
| (1)点燃一支蜡烛 | 蜡烛燃烧,发出黄色火焰 | |
| (2)取一个干而冷的烧杯罩在火焰上方 | 烧杯内壁上有水珠出现 | 蜡烛中一定含有 氢元素 |
| (3)迅速把烧杯倒转过来,往烧杯中倒入少量澄清石灰水 | 澄清石灰水变浑浊 | 化学方程式: CO2+Ca(OH)2═CaCO3↓+H2O |
| (4)用烧杯罩住点燃的蜡烛 | 蜡烛火焰熄灭 | 由此得知,燃烧必须具备的条件之一是 可燃物要与氧气接触 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
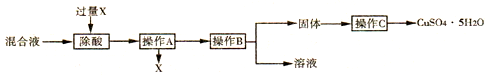
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 人体氟过量,易患龋齿 | B. | 含氟牙膏中的“氟”指氟单质 | ||
| C. | 该氟原子的相对原子质量近似为19 | D. | 该氟原子中有10个电子 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
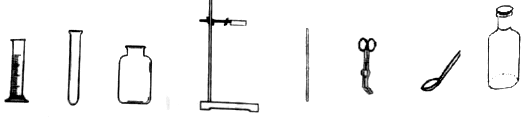
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com