
【题目】小明用如图装置进行实验。向充满二氧化碳的三个软质塑料瓶中分别注入等体积的饱和氢氧化钠溶液、饱和石灰水、水,立即拧紧瓶塞,振荡,观察现象。

(1)振荡B瓶的过程中观察到的现象是_______。
(2)小明观察到A瓶比C瓶变瘪得更明显,原因是________。
【答案】澄清石灰水变浑浊(澄清石灰水先变浑浊,后又变澄清)、瓶子变瘪 氢氧化钠和二氧化碳发生了反应(氢氧化钠吸收了二氧化碳)或等体积的氢氧化钠溶液比水吸收二氧化碳的量多
【解析】
(1)饱和的石灰水能和二氧化碳反应生成碳酸钙沉淀和水,则能观察到B中的溶液逐渐变浑浊。二氧化碳气体被吸收,瓶内压强减小,则能观察到B瓶变瘪。故答案为:澄清石灰水变浑浊(澄清石灰水先变浑浊,后又变澄清)、瓶子变瘪;
(2)A中盛放的是氢氧化钠溶液,C盛放的是水。二氧化碳能溶于水。当观察到A瓶比C瓶变瘪的更明显,则说明A中的氢氧化钠溶液可以吸收二氧化碳气体,使瓶内的压强更小。故答案为:氢氧化钠和二氧化碳发生了反应(氢氧化钠吸收了二氧化碳)或等体积的氢氧化钠溶液比水吸收二氧化碳的量多。


科目:初中化学 来源: 题型:
【题目】如图是某反应的微观示意图,下列说法错误的是
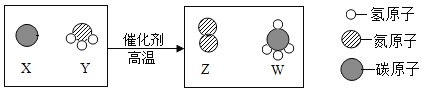
A.参加反应的X、Y两种物质的粒子个数之比为3:4
B.该反应不属于置换反应
C.W物质属于有机物
D.化学反应前后原子的种类、数目均保持不变
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】已知镁元素的原子结构示意图如图。请回答:
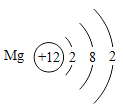
(1)镁原子的核电荷数为_____;
(2)镁元素的原子在化学反应中易____电子(填“获得”或“失去”),形成____离子(填“阴”或“阳”),镁离子的符号表示为____。
(3)由此可以得出:原子在失去最外层电子或在最外层得到电子达到稳定结构后,一定不会发生改变的有___。
①元素的种类;②元素的化学性质;③相对原子质量;④粒子的电性;⑤原子核;⑥最外层电子数;⑦电子层数;⑧核外电子总数;⑨质子个数。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】一定温度下,对固体甲的溶液进行恒温蒸发,实验记录如下:

根据上述实验,不能得到的结论是( )
A.①②溶液为不饱和溶液
B.固体甲在该温度下的溶解度为15g
C.固体甲的溶解度随温度的升高而增大
D.①~④溶液的溶质质量分数:①<②<③=④
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】84消毒液是生活中常用的一种消毒液,主要成分为次氯酸钠(NaClO)。实验小组对其进行研究。
(查阅资料)
Ⅰ. NaClO溶液呈碱性。
Ⅱ.消毒杀菌的原理是使菌体蛋白质变性,变性程度越大,消毒液消毒杀菌效果越好。鸡蛋清中的蛋白质发生变性反应时变为白色固体物质。
Ⅲ.ORP指84消毒液的漂白能力,ORP数值越大,84消毒液的漂白能力越强。
(进行实验)
实验1:制备84消毒液
某同学制作了一种84消毒液发生器(如图所示),用石墨作电极,电解饱和氯化钠溶液,即可制得消毒液。

实验2:在鸡蛋清中加入不同浓度的消毒液,静置15min现象如下表。
序号 | 2-1 | 2-2 | 2-3 | 2-4 |
实验 操作 |
|
|
|
|
实验现象 | 液体表面产生大量气泡,无其他现象 | 液体中产生大量白色固体 | 液体中产生少量白色固体 | 液体中产生极少量白色固体 |
实验3:探究84消毒液漂白性的影响因素
序号 | 3-1 | 3-2 |
实验操作 | 取烧杯倒入30mL浓度为1:100的84消毒液,将烧杯放置在距离光源 10cm处进行光照,测量ORP变化 | 取四个烧杯,分别倒入30mL浓度为1:100的84消毒液,并置于20°C、30°C、40°C、50°C水浴中加热,测量 ORP变化 |
测量数据 |
|
|
(解释与结论)
(1)实验1中,发生的主要反应如下,补全①的化学方程式。
①2NaCl+2H2O![]() 2NaOH+ Cl2↑+______ ↑ ②Cl2+2NaOH =NaCl+NaClO+H2O
2NaOH+ Cl2↑+______ ↑ ②Cl2+2NaOH =NaCl+NaClO+H2O
(2)实验2的目的是_______。
(3)实验3-1的结论是_______。
(4)根据实验3-2的测量数据可知,影响84消毒液漂白性的因素有_________。
(反思与评价)
(5)由实验3可知,84消毒液储存时需注意________。
(6)生活中,84消毒液不能与洁厕灵(主要成分是盐酸)混合使用的原因是________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列化学反应不属于置换反应的是
A.H2+ CuO![]() Cu + H2OB.2Mg + CO2
Cu + H2OB.2Mg + CO2 ![]() 2MgO + C
2MgO + C
C.CO + CuO![]() Cu + CO2D.2NaBr + Cl2 =2NaCl + Br2
Cu + CO2D.2NaBr + Cl2 =2NaCl + Br2
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】阅读下列材料,回答相关问题。
(材料1)2010 年 12 月 14 日下午,以“低碳生活”为主题的专题展览在中国科技馆正式开展。本次展览旨在引导公众改变生活观念,减少二氧化碳排放。展览共设 5 个分主题展区。
(1)地球村的“碳”危机,展示人类过度开发、高碳排放所造成的恶果,如温室气体产生的温室效应。二氧化碳、氧化亚氮(N2O)、甲烷和臭氧(O3)是地球大气中主要的温室气体,其中甲烷的化学式为___________。
(2)高科技的减“碳”术。为限制二氧化碳等温室气体的排放量,科学家采取“组合转化”技术,将二氧化碳和氢气在催化剂和加热条件下转化为一种重要的化工原料乙烯(C2H4)和水,该反应的化学方程式为_______________。
(3)新生活的低“碳”路。下列符合低碳生活理念的是___________(填序号)。
A少买不必要的衣服
B使用节能电器
C洗碗时不间断地放水冲洗
D少开私家车,多乘公共交通工具
(材料2)氨基钠(NaNH2)是合成维生素 A 的原料。工业上将钠于 97 ~ 100 ℃熔融,向反应容器中缓慢通入无水的液氨(NH3),再加热至 350 ~ 360 ℃生成氨基钠和氢气。
(1)下列说法中,正确的是______。
A钠可能与水反应
B钠的熔点比铁的熔点低
C维生素 A 中一定含有钠元素
(2)制备氨基钠的化学方程式为______。
(3)周期表中钠元素的信息如图所示,其原子的核外电子数为_____。

查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图为探究铝和铜的金属活动性强弱的实验先后图,下列说法不正确的是

A.反应后,铝片表面有紫红色固体生成
B.该反应为置换反应
C.反应后溶液比反应前的溶液质量增重了
D.根据该实验现象可以得出的铝活动性比铜强
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】化学兴趣小组的同学对“影响金属与盐酸反应的剧烈程度的因素”进行了探究:
[提出问题]金属与盐酸反应剧烈程度受哪些因素的影响?
[作出猜想]a、可能与金属本身的性质有关 b、可能与盐酸的浓度有关
[设计探究]实验所用金属均已用砂纸打磨
(1)实验①为探究猜想a,小组同学分别在两支试管中放入相同质量的锌片和铁片,然后分别加入相同浓度,相同质量的稀盐酸,观察到放锌片的试管中立即产生大量气泡,放铁片的试管中只产生少量气泡,铁和稀盐酸反应的化学方程式为__________。从实验现象可判断:金属活动性Zn_______Fe (填“<”“=”“>”)。
得出结论:金属与盐酸发生反应的剧烈程度与金属本身性质有关,金属的活动性与反应的剧烈程度的关系是________。
(2)实验②为探究猜想b,小组同学设计如图的装置进行实验,其中注射器的作用是_________。

所用药品,实验数据如下表:
实验编号 | 选用金属(均取2g) | 盐酸质量分数(均取50mL) | 每分钟产生氢气的体积/mL | |||||
1分|钟 | 1~2分钟 | 2~3分钟 | 3~4分钟 | 4~5分钟 | 前5分钟共收集气体 | |||
Ⅰ | 锌片 | 15% | 2.9 | 16.9 | 11.0 | 9.2 | 7.6 | 48.5 |
Ⅱ | 锌片 | 5% | 1.6 | 8.4 | 5.9 | 4.8 | 3.7 | 24.4 |
(3)得出结论:金属与盐酸发生反应的剧烈程度与盐酸的浓度有关,其关系是__________。
(4)[反思评价]根据表中实验II数据分析,锌与盐酸发生反应快慢的变化情况为________,其原因为_______。
(5)通过以上探究,你认为金属与盐酸反应的剧烈程度可能还受哪些因素的影响_______(写一条即可)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com