
【题目】实验室需配制一定溶质质量分数的溶液。
(1)配制100mL质量分数为10%的氢氧化钠溶液(密度为1.1g/cm3),所需氢氧化钠的质量为_____g,所需蒸馏水的体积为_____mL(水的密度为lg/cm3)。
(2)用氢氧化钠固体配制10%的氢氧化钠溶液过程中,需要用到的仪器除了托盘天平、药匙、量筒、烧杯、玻璃棒、试剂瓶外,还需要_____。
(3)下列操作正确的是_____。
A称量氢氧化钠固体时,左盘放砝码
B将准确称量的氢氧化钠固体放入装有水的量筒中溶解
C将配制好的氢氧化钠溶液装入试剂瓶中,塞好瓶塞并贴上标签
D称量时,先添加所需的氢氧化钠,再移动游码直到天平平衡
(4)把10%的氢氧化钠溶液加水配制为150g质量分数为8%的氢氧化钠溶液,需水的质量为_____g。
【答案】11 99 胶头滴管 ABD 30
【解析】
(1)配制100mL质量分数为10%的氢氧化钠溶液(密度为1.1g/cm3),所需氢氧化钠的质量=100mL×1.1g/cm3×10%=11g;水的质量为110g-11g=99g,故水的体积=![]() 合99mL;
合99mL;
(2)用氢氧化钠固体配制10%的氢氧化钠溶液过程中,需要用到的仪器除了托盘天平、药匙、量筒、烧杯、玻璃棒、试剂瓶外,还需要胶头滴管;
(3)A 称量氢氧化钠固体时,应在右盘放砝码,故A错误;
B将准确称量的氢氧化钠固体放入装有水的烧杯中溶解,不可在量筒内配制溶液,故B错误;
C将配制的氢氧化钠溶液装入试剂瓶中,塞好瓶塞并贴上标签,故C正确;
D 称量时,先添加砝码和移动游码,再添加氢氧化钠直到天平平衡,故D错误;故选ABD;(4)设:需水的质量为x。150g×8%=(150g-x)×10% x=30g。把10%的氢氧化钠溶液加水配制为150g质量分数为8%的氢氧化钠溶液,需水的质量为30g。


科目:初中化学 来源: 题型:
【题目】实验室常用下列装置来制取气体:
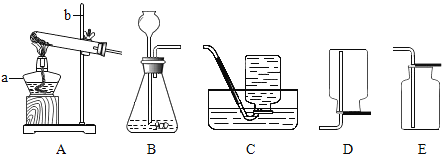
(1)写出图中有标号仪器的名称:a_____ b_____;
(2)实验室常用B、C或B、E装置组合来制备某气体,写出制备某气体的反应化学方程式:_____;能用B、E组合来制备的气体还有_____.
(3)用高锰酸钾制取氧气时,发生反应的化学方程式为_____.
(4)用E装置收集氧气的依据是_____,检验氧气是否集满的方法是_____.
(5)实验室常用氯化铵固体与碱石灰固体共热来制取氨气.常温下NH3是一种无色、有刺激性气味的气体,密度比空气小.NH3极易溶于水,其水溶液呈碱性.
①制取氨气反应的方程式:![]() .X的化学式为:_____.
.X的化学式为:_____.
②制取并收集NH3,应该从图中选择的发生装置是_____,收集装置是_____.
③NH3是一种碱性气体,干燥时不能选用下列干燥剂中的_____(填序号).
A 固体氢氧化钠 B 浓硫酸 C 生石灰
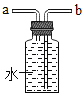
(6)用如图所示装置收集氧气,氧气应从_____(填“a”或“b”)端导入;
(7)要鉴别氧气和二氧化碳,可选择_____.
A 无色酚酞溶液 B 紫色石蕊溶液
C 澄清石灰水 D 燃着的木条.
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】实验是进行科学探究的重要途径.
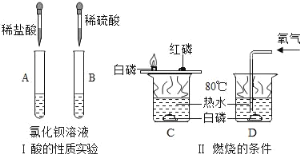
(1)下列实验仪器不能用作反应容器的是_____(填字母序号).
A.烧杯 B.试管 C.量筒 D.锥形瓶
(2)根据下面2个实验装置示意图回答相关问题.
①实验Ⅰ两支试管中出现现象的不同之处是_____,通过实验可认识到:虽然酸类物质具有相似的化学性质,但由于不同的酸溶于水时电离出的_____不同,其性质也存在差异.
②变量控制是科学研究常用的方法,例如我们在实验室做检验CO2的溶解性实验时需控制两个因素:一是两个塑料容器的容积相同,二是容器中加入的水量相同,则实验Ⅱ中控制的两个因素分别是_____、_____.
(3)某同学将一枚洁净的铁钉放入硫酸铜溶液中,观察到铁钉表面有红色的物质析出,且产生少量的气体,于是,他重新配制硫酸铜溶液,再次实验,又观察到相同的现象,请回答下列问题:
①产生的气体可能是_____;②由实验可以得出两种金属的活动性顺序是_____.
(4)用1000t含氧化铁80%的赤铁矿石炼铁,理论上可以炼出含铁96%的生铁质量是多少?
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图所示为实验室常见气体制备、净化、干燥、收集和性质等实验的部分仪器,某校化学实验小组的同学完成下列实验探究:
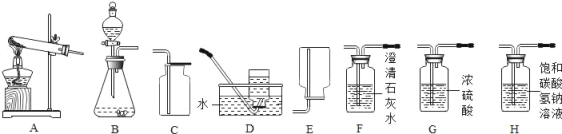
①一组同学欲制取硫化氢气体:查阅资料知,通常情况下,硫化氢气体是一种无色有臭鸡蛋气味的有毒气体,密度比空气大,能溶于水,其水溶液叫氢硫酸(H2S)。实验室用硫化亚铁固体与稀盐酸反应制取硫化氢气体时,应选择的发生装置为_____(填字母),能否用D装置收集硫化氢气体,并说明理由_____。为了防止中毒和污染空气,多余的硫化氢气体可用氢氧化钠溶液吸收,其反应的化学方程式为_____(氢硫酸跟稀盐酸一样,能与碱发生中和反应)。
②二组同学以石灰石和稀盐酸为原料,制备并收集一瓶干燥、纯净的二氧化碳气体,按照要求设计实验装置、连接仪器,并检验装置的气密性。所选仪器的连接顺序应为_____(填写字母序号),用化学方程式表示饱和NaHCO3溶液的作用_____。若将二氧化碳通入澄清的石灰水中,写出发生反应的化学方程式_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】根据下列装置图回答问题:
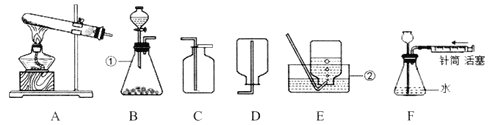
(1)写出标号仪器的名称:①_____,②_____。
(2)实验室用高锰酸钾制取氧气的化学方程式为_____;如用E装置收集氧气,当观察到_____时,再把导管口伸入盛满水的集气瓶里。
(3)乙炔(C2H2)是重要的化工原料。实验室用电石(CaC2块状固体)与水反应来制取乙炔气体,应选用的发生装置是_____。
(4)小明同学用B、C装置组合制取二氧化碳,当用燃着的小木条放在C装置瓶口时,发现小木条始终不熄灭,说明气体没有集满,可能的原因是_____。
(5)检查F装置气密性的方法是:当把针筒中的活塞内推后,静置观察,若看到_____,说明气密性良好。
(6)实验室用锌与浓盐酸反应制取纯净、干燥的氢气,可将制得的气体先通过盛有________的洗气瓶,再通过盛有_____的洗气瓶。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】可燃冰的分子结构类似于笼形,即若干个水分子将甲烷分子包裹在里面,其化学式为CH4·nH2O,n一般为6-8。仅我国南海可燃冰提供的能源就够中国用80年以上。
(1)甲烷是一种____(填“无机化合物”或“有机化合物”),属于____(填“可”或“不可”)再生能源。我国的可燃冰开采技术世界领先,若甲烷大量泄露到大气中,会加剧__(填一种大气危害现象)的产生;甲烷燃烧的化学方程式为__。
(2)海底的CH4在0℃、30个大气压的条件即可生成可燃冰,该反应的化学方程式是____;若n=8时,其中碳元素质量分数是____。
(3)可燃冰燃烧时能量转化形式主要是化学能转化为____能,而CH4—O2燃料电池则是将化学能转化为____能的装置;
(4)我国于2017年4月成功开采获取可燃冰,其意义在于____。
a.促进我国能源结构的快速转型
b.有助于中国在可燃冰可采和利用领域具备一定的话语权
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】20℃时,将等质量的a、b两种固体,分别加入到盛有l00g水的烧杯中,充分搅拌后,现象如图甲,升温到50℃时,现象如图乙,a、b两种固体的溶解度曲线如图丙。下列说法不正确的是
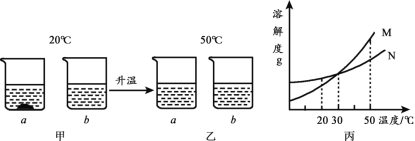
A. 图丙中M表示a的溶解度曲线 B. 图甲溶液中溶质的质量分数a大于b
C. 图乙溶液中b溶液一定不饱 和 D. 30℃时a、b溶解度相等
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】为探究铁的化学性质,某学习小组做了如图甲所示实验。他们观察到试管a中铁粉全部溶解,产生大量气泡,溶液呈①____色,反应的化学方程式为②____;试管b中有③______色固体生成,该反应的化学方程式为④_____。为进一步确定试管a所得溶液中的溶质成分和试管b所得固体的组成,他们进行了以下实验探究。
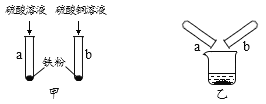
(提出猜想)(1)试管a中的溶质成分:猜想一:FeSO4;猜想二:⑤______。
(2)试管b中固体的组成:猜想三:Cu; 猜想四:Fe和Cu。
(实验探究)甲图所示实验结束后,将试管a、试管b内的物质全部倒入同一烧杯中(如乙图所示),他们惊奇地发现烧杯内溶液中产生大量气泡。
(总结交流)经过讨论,大家一致认为上述猜想中正确的是⑥_______。
(拓展探究)某混合溶液由硫酸铜和硫酸溶液组成。上述小组同学取192.4g该混合溶液于烧杯中,然后往其中加入33.6g铁粉,充分混合后,恰好完全反应。实验测得反应过程中产生气体的质量为0.4g。计算:
(3)原混合溶液中H2SO4的质量______。(计算结果保留一位小数)
(4)原混合溶液中CuSO4和H2SO4的质量比______。
(5)完全反应后所得溶液中溶质的质量分数_______。(计算结果保留一位小数)
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】有一含有纯碱的食盐样品,为了测定其中碳酸钠的含量,某同学称取10g的样品放入烧杯中,向烧杯中加入100g足量的 稀盐酸,充分反应后气体全部逸出,烧杯中剩余物的总质量为109.56g(假设产生的气体全部逸出。以下计算结果保留一位小数)
(1)样品中碳酸钠的含量是___
(2)NaCl中氯元素质量分数是____
(3)反应后溶液中溶质质量分数是___?
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com