

分析 根据给出的转化关系对应的过程分析每个对应的问题,或者直接分析每个问题,从给出的信息中找对应的信息.
III根据质量守恒定律可知,总质量的减少量就是生成氢气的质量,根据生成氢气的质量和对应的化学方程式可求参加反应的单质铁的质量,进而求算其质量分数.
解答 解:
Ⅰ、地壳中元素含量由高到低的几种元素为:氧硅铝铁,所以含量最多的金属元素是 铝.
Ⅱ、
(1)过程③是铁和硫酸铜反应生成硫酸亚铁和铜,对应的化学方程式是 Fe+CuSO4=FeSO4+Cu.
(2)光亮铁钉生锈是和氧气和水反应,所以质量增加了;而生锈的铁钉和稀盐酸反应,导致表面的锈被反应掉,所以无锈铁钉质量小于生成的铁钉,同时由于转化为铁锈的那部分铁元素进入了溶液,所以无锈铁钉的质量也小于光亮铁钉;无锈铁钉和硫酸铜反应时,每56份质量铁钉反应生成64份质量的铜附着在铁的表面,铁钉质量增加,所以红色铁钉的质量比无锈铁钉质量答,所以在光亮铁钉、生锈铁钉、无锈铁钉、红色“铁钉”中质量最小的是 无锈铁钉.
III、根据质量守恒定律可得,生成的氢气的质量为10g+100g-109.7g=0.3g
设生锈铁钉中单质铁的质量为x
Fe+2HCl=FeCl2+H2↑
56 2
x 0.3g
$\frac{56}{2}$=$\frac{x}{0.3g}$
x=8.4g
生锈铁钉中单质铁的质量分数为$\frac{8.4g}{10g}$×100%=84%
故答案为:Ⅰ、铝.
Ⅱ、
(1)Fe+CuSO4=FeSO4+Cu.
(2)无锈铁钉.
Ⅲ、84%
点评 根据化学方程式计算时,第一要正确书写化学方程式,第二要使用正确的数据,第三计算过程要完整.


 红果子三级测试卷系列答案
红果子三级测试卷系列答案 课堂练加测系列答案
课堂练加测系列答案科目:初中化学 来源: 题型:选择题
| A. | 它是由C、H、O、N四种元素组成的 | B. | 碳酸氢铵适宜在晴朗的天气下使用 | ||
| C. | 碳酸氢铵不稳定,受热易分解 | D. | 碳酸氢铵适宜低温、避光、密封保存 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A化学反应基本类型 | B化学反应中常见的“三” |
| ①化合反应:4P+5O2$\frac{\underline{\;点燃\;}}{\;}$2P2O5 ②分解反应:H2CO3═H2O+CO2↑ ③复分解反应:CO2+2NaOH=Na2CO3+H2O | ①煤、石油、天然气-三大化石燃料 ②塑料、合成纤维、合成橡胶-三大合成材料 ③分子、原子、离子-构成物质的三种粒子 |
| C对鉴别方法的认识 | D化学与生活 |
| ①区分氮气和氧气-伸入带火星的木条 ②区分硬水和软水-加肥皂水 ③区分硫酸铵和氯化铵-加熟石灰粉末研磨 | ①用氢氧化钠改良酸性土壤 ②缺乏维生素C易患坏血病 ③缺乏碘元素易患甲状腺肿大 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| 加入物质 | BaCl2溶液 | CuO固体 | NaCl溶液 |
| 现象 | 产生白色沉淀 | 固体溶解,溶液变蓝 | 无明显现象 |
| A. | AgNO3溶液 | B. | 稀硫酸 | C. | NaOH溶液 | D. | K2CO3溶液 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 硝酸铵固体放于水中,迅速溶解且溶液温度降低 | |
| B. | 铵态氮肥与碱共热放出无色无味气体 | |
| C. | 用pH试纸测得某溶液的pH=1.4 | |
| D. | 盐酸滴入紫色石蕊试液中,盐酸变成红色 |
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
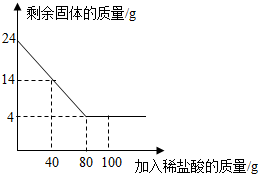 某化学兴趣小组为了测定当地的石灰石(主要成分是CaCO3)的质量分数,他们做了如下实验:取24克样品放入烧杯中,向其中逐渐加入100克一定质量分数的稀盐酸(杂质不溶于水也不与酸反应),所用盐酸的质量分数与剩余固体的质量关系如图所示,请根据图中的数据进行计算:
某化学兴趣小组为了测定当地的石灰石(主要成分是CaCO3)的质量分数,他们做了如下实验:取24克样品放入烧杯中,向其中逐渐加入100克一定质量分数的稀盐酸(杂质不溶于水也不与酸反应),所用盐酸的质量分数与剩余固体的质量关系如图所示,请根据图中的数据进行计算:查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 二氧化碳和氮气 | B. | 氮气和水蒸汽 | ||
| C. | 一氧化碳和二氧化碳 | D. | 氮气和氢气 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com