
| 实验步骤 | 实验现象 | 实验结论 |
| 取适量镉、铜、银于试管中,加入足量盐酸 | 镉表面有气泡产生,铜、银表面无气泡产生 | 镉的活动性顺序大于铜与银 |
| 取适量铜于试管中,加入少量硝酸银溶液 | 有银白色固体析出 | 铜的活动性顺序大于银 |
分析 根据已有的知识进行分析解答,在金属活动性顺序中,氢前的金属能与酸反应产生氢气,位置在前的金属能将位于其后的金属从其盐溶液中置换出来,据此解答.
解答 解:(1)镉表面有气泡产生,则说明加入的是酸,故填:盐酸;
铜的活动性强于银,故取适量铜于试管中,加入少量硝酸银溶液,会观察到有银白色的固体析出,故填:有银白色固体析出;
(2)氯化镉能与氢氧化钠反应生成氢氧化镉沉淀和氯化钠,由于氢氧化钠具有极强的腐蚀性,会造成水体污染,故可以用熟石灰氢氧化钙代替氢氧化钠,故填:CdCl2+2NaOH=Cd(OH)2↓+2NaCl;氢氧化钠具有极强的腐蚀性;熟石灰.
点评 本题考查的是金属活动性顺序的探究,完成此题,可以依据已有的金属活动性顺序的意义进行.


 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:选择题
| A. | 酸碱一定含有氧元素,盐一定含有氧元素 | |
| B. | 碱盐可能含有氧元素,酸一定含有氧元素 | |
| C. | 盐一定含有金属元素,酸碱不一定含有金属元素 | |
| D. | 酸碱一定含有氢元素,盐不一定含有金属元素 |
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
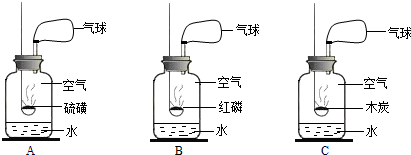
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
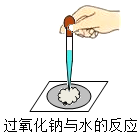 过氧化钠是一种淡黄色的固体,某同学在探究过氧化钠性质时,做了如图实验:用棉花包住少量的过氧化钠固体放在石棉网上,然后向棉花上滴加3~4滴水;发现:棉花剧烈燃烧起来.小明根据燃烧的条件,对该反应做出了大胆猜想:
过氧化钠是一种淡黄色的固体,某同学在探究过氧化钠性质时,做了如图实验:用棉花包住少量的过氧化钠固体放在石棉网上,然后向棉花上滴加3~4滴水;发现:棉花剧烈燃烧起来.小明根据燃烧的条件,对该反应做出了大胆猜想:查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题

查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| 需区分物质 | 方法一 | 方法二 | |
| A | 空气和氧气 | 用带火星木条检验 | 闻气味 |
| B | 硬水和软水 | 观察颜色 | 加明矾搅拌 |
| C | 铜丝和铁丝 | 用磁铁吸引 | 观察颜色 |
| D | 二氧化碳和氮气 | 澄清石灰水 | 燃着的木条 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com