(2011?天门)“如何验证无明显现象化学反应的发生”是以下学习片段的主题,请参与其中并完成下列问题.
[知识回顾]向AlCl
3溶液中滴加少量的KOH溶液,产生白色沉淀,其反应的化学方程式为
AlCl3+3NaOH=Al(OH)3↓+3NaCl
AlCl3+3NaOH=Al(OH)3↓+3NaCl
.
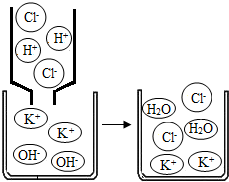
[设疑提问]KOH溶液与盐酸混合无明显现象,如何设计实验验证KOH溶液与盐酸发生了反应?
[实验方法]
方法一:向滴有酚酞的KOH溶液中加入盐酸,溶液颜色
红色逐渐变为无色
红色逐渐变为无色
,表明反应发生.
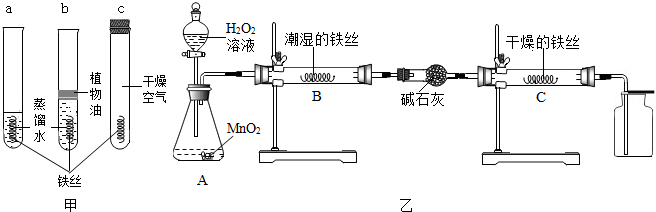
方法二:直接将KOH溶液与盐酸混合后,向其中加入铁丝,可能有两种情况:
(1)当加入铁丝无气泡产生时,说明二者发生了反应,理由是
如有气泡,则有盐酸
如有气泡,则有盐酸
.
(2)当加入铁丝有气泡产生时,不能判断二者发生了反应,理由是
可能盐酸剩余
可能盐酸剩余
.因此,“验证无明显现象化学反应的发生”往往可以通过加入某种合适的试剂来指示,方法二不合理,加入的物质不能准确指示反应的发生.
[问题延伸]KOH溶液与盐酸发生了中和反应,从图中可知反应的实质是
H+和OH-结合生成H2O分子
H+和OH-结合生成H2O分子
.
[知识拓展]KOH溶液与CO
2反应也无明显现象,而用酚酞溶液却不能指示该反应的发生,原因是
氢氧化钾和碳酸钾溶液都为碱性
氢氧化钾和碳酸钾溶液都为碱性
.
信息:碳酸钾是草木灰的主要成分,草木灰不宜与铵盐混合施用.

 ,则该粒子的符号是
,则该粒子的符号是

 (2011?天门)“如何验证无明显现象化学反应的发生”是以下学习片段的主题,请参与其中并完成下列问题.
(2011?天门)“如何验证无明显现象化学反应的发生”是以下学习片段的主题,请参与其中并完成下列问题.