(2013?丰台区一模)某学习小组对在实验中吸收过二氧化碳气体的碱石灰成分进行了研究.
【查阅资料】
①碱石灰是CaO与NaOH 的固体混合物,通常用于吸收二氧化碳及干燥气体.
②碱性的Na
2CO
3溶液可以与中性的CaCl
2溶液发生复分解反应.
【提出猜想】
该碱石灰的主要成分可能含有
CaO
CaO
、Ca(OH)
2、CaCO
3、NaOH和
Na2CO3
Na2CO3
.
【设计方案、收集证据】
(1)甲同学在烧杯中放入少量的碱石灰样品,加入足量蒸馏水充分搅拌,静置有白色沉淀,甲同学认为样品中一定含有CaCO
3,乙同学认为他的结论不准确,原因是:
Na2CO3+Ca(OH)2=CaCO3↓+2NaOH
Na2CO3+Ca(OH)2=CaCO3↓+2NaOH
(填化学方程式).
(2)乙同学进一步设计实验并进行验证,过程如下:
| 实验操作 |
实验现象 |
实验结论 |
| ①从甲同学的烧杯中取少量上层清液于试管中,向其中滴加足量 CaCl2 CaCl2 溶液. |
有白色沉淀生成 |
生成白色沉淀的化学方程式为:
Na2CO3+CaCl2=CaCO3↓+2NaCl Na2CO3+CaCl2=CaCO3↓+2NaCl . |
| ②过滤,向滤液中滴加无色酚酞试液. |
无明显现象 |
通过实验及分析,样品中不含有:
Ca(OH)2、NaOH和CaO Ca(OH)2、NaOH和CaO . |
【解释与评价】
(1)乙同学进一步设计了下列实验装置,通过称量B装置的质量变化来确定样品的成分及质量(气密性良好,每步均完全反应,操作无误).
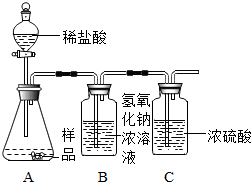
多次实验发现测定结果有时偏大有时偏小偏差,试分析其主要原因:
锥形瓶中残留的CO2未被吸收会导致结果偏小,而挥发出来的氯化氢及空气中二氧化碳和水蒸气被吸收则会导致结果偏大;每次实验两种因素综合作用,残留的CO2质量大于挥发出来的氯化氢及空气中二氧化碳水蒸气质量导致结果偏小,反之则导致偏大
锥形瓶中残留的CO2未被吸收会导致结果偏小,而挥发出来的氯化氢及空气中二氧化碳和水蒸气被吸收则会导致结果偏大;每次实验两种因素综合作用,残留的CO2质量大于挥发出来的氯化氢及空气中二氧化碳水蒸气质量导致结果偏小,反之则导致偏大
.
(2)在老师的指导下乙同学完善了实验装置,并重新进行了实验,步骤如下:
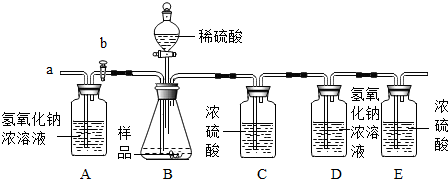
①检查装置气密性,将5.06g干燥的样品放入锥形瓶中;
②打开活塞b,从导管a处缓缓鼓入一定量的空气,关闭活塞b;
③称量盛有氢氧化钠浓溶液的D瓶质量;
④向锥形瓶中逐滴加入稀硫酸至不再产生气泡;
⑤打开活塞b,从导管a处缓缓鼓入一定量的空气;
⑥称量D瓶质量,增重2.2g.
通过分析及计算可知:5.06g样品中各成分及质量
CaCO3:4克Na2CO3:1.06g.
CaCO3:4克Na2CO3:1.06g.
.




