
【题目】化学就在我们身边,请用所学化学知识回答下列问题。
(1)金刚石和石墨都是由_______组成的单质,但是它们物理性质存在着较大差异的原因是_________;
(2)用一氧化碳和磁铁矿石(主要成分是Fe3O4)炼铁,其反应的化学方程式是_______________;
(3)制造列车使用了大量的铝合金材料,铝合金的硬度比纯铝的硬度_____________;在空气中,铝制品耐腐蚀的原因是_________________。
【答案】碳元素 碳原子的排列方式不同 4CO + Fe3O4![]() 3Fe +4CO2 大 常温下,铝与氧气反应生成一层致密的氧化铝薄膜
3Fe +4CO2 大 常温下,铝与氧气反应生成一层致密的氧化铝薄膜
【解析】
(1)金刚石和石墨都是由碳元素组成的单质,二者的物理性质存在着较大差异的原因是它们的碳原子的排列方式不同,故填:碳元素;碳原子的排列方式不同;
(2)用一氧化碳和磁铁矿石(主要成分是Fe3O4)炼铁,二者反应生成铁和二氧化碳,条件是高温,其反应的化学方程式为4CO+Fe3O4![]() 3Fe+4CO2,故填:4CO+Fe3O4
3Fe+4CO2,故填:4CO+Fe3O4![]() 3Fe+4CO2;
3Fe+4CO2;
(3)合金的硬度大于其成分金属,铝合金的硬度比纯铝的硬度大;在空气中,铝制品耐腐蚀的原因是铝易被氧气氧化生成致密的氧化铝保护膜,故填:大;常温下,铝与氧气反应生成一层致密的氧化铝薄膜。


科目:初中化学 来源: 题型:
【题目】物质王国举行一场趣味篮球赛。某队由铁、二氧化碳、硫酸、氢氧化钙、氯化铜五名“队员”组成,比赛中,由氯化铜“队员”发球,“队员”间传接球,最后由D位置“队员”投篮进球完成一次有效进攻。场上“队员”位置及传球路线如图所示。
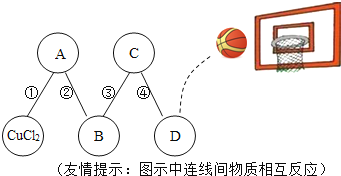
(1)已知D位置上投篮的“队员”是个灭火“能手”,则D位置“队员”代表的物质是________;
(2)B位置“队员”所代表物质的一种用途是________;
(3)写出连线④代表的物质间发生反应的化学方程式________;连线①代表的物质间发生化学反应的基本类型是________反应。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】电影《复仇者联盟》中,美国队长和蜘蛛侠使用的武器和衣服如图所示,请回答下列问题:

(1)图中标示的物质中,属于金属材料的是______________,属于有机合成材料的是___________。
(2)艾德曼合金钢属于____________(填纯净物或混合物),其含有主要元素是_____________(填元素符号),它与生铁的区别是________。
(3)科技的进步促进材料的发展,请你谈一谈化学材料与生活的关系_________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下图是实验室中常见装置,回答下列问题。
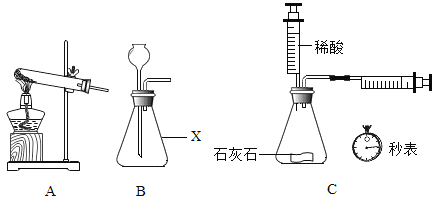
(1)仪器X的名称是______________。
(2)实验室用氯酸钾制取O2应选用的发生装置是______ ( 填字母序号)反应的化学方程式是______________,该反应属于______________(填反应类型)。
(3)利用图C装置探究不同地区石灰石与酸反应的剧烈程度。选用规格大小相同的不同地区的石灰石与等体积稀酸反应,从酸的角度说明还需要控制的变量有______________,实验时通过测定_____________来比较。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】武汉举行首届中国国际钢铁流通博览会,将商讨全球金属流通行业的战略性问题。则回答:
(1)金属材料的生产和使用是人类文明和社会进步的重要标志。常见三种金属铜、铁和铝被先后大规模的发现与使用,则其中的原因是(_____)
A 地壳中金属元素的含量 B 金属的导电性
C 金属的活动性顺序 D 金属的资源与价格
(2)大型钢铁企业常以焦炭、赤铁矿(主要成分是氧化铁)、空气等为主要原料炼铁,相关系列的化学反应过程如下:
![]()
请写出第①②步反应的化学方程式分别为_______________和__________。第③步反应的反应现象为______________________________。
(3)金属矿物的储量有限,而且不能再生。目前世界上已有50%以上的废钢铁得到回收利用,请说明其目的是________(填“合理开采矿物”、“节约金属资源”或“开发出金属的代用品”)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】高纯硅是制造计算机芯片的重要材料。如图是元素周期表中硅元素的相关信息及原子结构示意图,下列说法正确的是( )
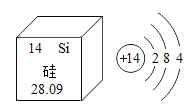
A. 硅元素属于金属元素
B. 硅原子核外有4个电子
C. 硅的相对原子质量为28.09
D. 硅原子在化学反应中易失电子
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某品牌粉笔的成分为碳酸钙、硫酸钙,可能含有少量氧化钙。取37g干燥的粉笔研磨成粉末,加入足量稀盐酸,充分反应后得到8.8g气体。将反应后的固液混合物蒸干,测得其中钙元素质量为13.5g。(说明:硫酸钙与稀盐酸不反应)
(1)根据化学方程式计算37g粉笔中碳酸钙的质量。
(2)推断该粉笔中是否含有氧化钙。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】过氧化镁(MgO2)是一种镁精细化工产品。在医疗上可用来治疗消化不良、胃酸过多等疾病。在环境保护方面,过氧化镁可用来处理地下水污染的土壤。还可以用于牙膏,对牙齿有漂白和防过敏的作用。某化学兴趣小组对过氧化镁的性质和制备等进行了以下研究。
一.过氧化镁的性质
(1)过氧化镁(其中氧元素的化合价为____)是一种白色的粉末,其外观与物理性质与氧化镁相似。化学性质不够稳定,不溶于水,但逐渐的被分解放出氧气。
过氧化镁有强氧化性,常温下比较稳定,但是加热时会分解生成氧气和氧化镁。请下出该反应的化学方程式________。
(2)过氧化镁易溶于稀盐酸,发生反应:MgO2+2HCl=MgCl2+H2O2同时温度升高,说明该反应热量__________(填“放出”或“吸收”)。
二.过氧化镁的制备
下图是利用碱式碳酸镁(Mg2(OH)2CO3)和30%的过氧化氢溶液来制取过氧化镁。
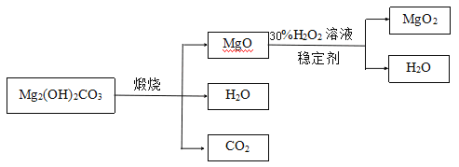
(资料)①碱式碳酸镁与碳酸镁有相似的化学性质,能与稀盐酸反应产生二氧化碳②氧化镁与过氧化氢反应放出大量的热
(3)检测煅烧过程碱式碳酸镁完全分解的方法是_________(写出具体的操作和现象);上述生产过程加入稳定的剂的作用是________。
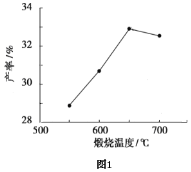
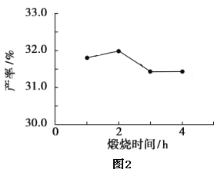
(4)用上述碱式碳酸镁在550、600、650及700℃下煅烧一定的时间生成氧化镁。用上述条件制备的氧化镁分别与30%双氧水反应合成过氧化镁产率(见图1和图2)。
碱式碳酸镁煅烧的温度适宜控制在________℃,煅烧的时间适宜控制在______h。
(5)结果在适宜的温度和时间下,碱式碳酸镁能完全分解,并且得到的氧化镁颗粒表面积最大,能与30%过氧化氢充分反应,所以产率高。推测700℃时,产率明显降低的可能的原因____。
三.过氧化镁产品纯度检测
在生产过程中,过氧化镁中常常含有少量的氧化镁杂质(其他杂质不考虑),以下是该小组进行纯度检测的实验装置和实验步骤。

①检查装置气密性,装入药品(样品质量为0.7g),调节刻度管使左右两边液面相平,刻度管度数为10.0mL。
②打开分液漏斗开关,待瓶中无气泡产生时,关闭开关。
③再次调节刻度管使左右两边液面相平,刻度管度数为122mL。
(6)稀盐酸中放入的少量硫酸铜溶液目的是__________。
(7)根据上面实验数据计算样品中过氧化镁的质量分数__________(写出具体的计算过程,实验条件下O2密度为1.429g/L)。
(8)该小组同学所测得质量分数比实际结果偏大,你觉得可能的原因是(_______)
A 生成的氧气有少量溶于水 B 未等装置冷却到室温就开始读数
C 杂质与盐酸反应能产生少量的气体 D 滴入的稀盐酸占了一部分气体的体积
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】二氧化碳的捕捉与封存是实现温室气体减排的重要途径之一,科学家利用NaOH溶液喷淋“捕捉”空气中的CO2(如图).则关于该方法的叙述不正确的是( )
A. 该方法中包含三种基本化学反应类型
B. 物质①是NaOH溶液
C. 操作①是蒸发浓缩、降温结晶
D. 该方法需要消耗一定的能源
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com