
| A. | 苯丙氨酸由23个原子构成 | |
| B. | 苯丙氨酸分子由碳、氢、氧、氮四种元素组成 | |
| C. | 苯丙氨酸为有机物,明胶为混合物 | |
| D. | 苯丙氨酸中碳、氢、氧氮元素的质量比为9:11:2:1 |
分析 A、根据苯丙氨酸是由分子构成的进行解答;
B、根据分子是由原子构成的,物质是由元素组成的进行解答;
C、根据有机物和混合物的定义进行解答;
D、根据化合物中元素质量比的计算方法来分析.
解答 解:A、苯丙氨酸是由苯丙氨酸分子构成的,苯丙氨酸分子是由原子构成的,故A错误;
B、苯丙氨酸分子由碳原子、氢原子、氧原子、氮原子构成的,故B错误;
C、含有碳元素的化合物为有机物,故苯丙氨酸为有机物正确,明胶里含有多种蛋白质,故明胶为混合物正确,故C正确;
D、由苯丙氨酸的化学式C9H11O2N可知,碳、氢、氧、氮四种元素的质量比为:12×9:1×11:16×2:14=108:11:32:14≠9:11:2:1,故D错误.
故选C.
点评 本题难度不大,考查了化学式的含义、有关化学式的简单计算等知识,灵活运用所学知识解答实际问题是解题的关键.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:初中化学 来源: 题型:解答题

| 实 验 步 骤 | 实验现象 | 结论或解释 |
| (1)打开干电池,取出碳棒周围的黑色粉末. | / | / |
| (2)将粉末置于烧杯内,加入适量水溶解、过滤、洗涤、干燥 | 得到黑色粉末和无色澄清液体 | 黑色粉末的成份为二氧化锰和炭粉 |
| (3)对黑色粉末进行灼烧 | / | 得到纯净的MnO2固体 |
| (4)取少量第(2)步中得到的无色澄清液体于试管,检验第②步中得到的无色澄清液体中是否含铵根离子的方法是:取样于试管中,加入氢氧化钠溶液并加热(把湿润的红色石蕊试纸放在试管口) | 强烈刺激性气味(或湿润的红色石蕊试纸变蓝色) | 结论:无色溶液中含铵根离子.化学方程式为: NH4Cl+NaOH═NaCl+H2O+NH3↑ |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:解答题
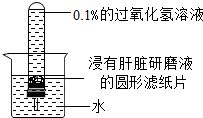 陈奇同学为研究肝脏研磨液中过氧化氢酶对过氧化氢分解的
陈奇同学为研究肝脏研磨液中过氧化氢酶对过氧化氢分解的查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
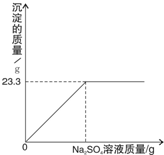 (称取NaCl和BaCl2的固体混合物32.5g,加入100g蒸馏水,完全溶解后向该混合溶液中逐滴加入质量分数为10%的Na2SO4溶液,反应生成BaSO4沉淀的质量与所加入的Na2SO4溶液的质量关系如下图所示.试回答下列问题:
(称取NaCl和BaCl2的固体混合物32.5g,加入100g蒸馏水,完全溶解后向该混合溶液中逐滴加入质量分数为10%的Na2SO4溶液,反应生成BaSO4沉淀的质量与所加入的Na2SO4溶液的质量关系如下图所示.试回答下列问题:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com