
| A. | BaSO4 | B. | MgO | C. | CaCO3 | D. | Cu |
分析 盐的溶解性规律:钾盐钠盐铵盐硝酸盐都可溶;盐酸盐中不溶氯化银;硫酸盐中不溶硫酸钡;碳酸盐只溶钾盐、钠盐、铵盐;据此根据常见盐的溶解性、酸与盐的化学性质进行分析判断.
解答 解:盐的溶解性规律:钾盐钠盐铵盐硝酸盐都可溶;盐酸盐中不溶氯化银;硫酸盐中不溶硫酸钡;碳酸盐只溶钾盐、钠盐、铵盐.
A、BaSO4难溶于水,又不溶于稀盐酸,也不与硝酸银溶液反应,故选项错误.
B、MgO难溶于水,但能与稀盐酸反应生成氯化镁和水,能溶于酸,故选项错误.
C、碳酸钙难溶于水,但能与稀盐酸反应生成氯化钙、水和二氧化碳,能溶于酸,故选项错误.
D、铜难溶于水,不能与稀盐酸反应;能与硝酸银溶液反应生成硝酸铜溶液和银,故选项正确.
故选:D.
点评 本题难度不大,主要考查常见物质的水溶性,熟记常见盐的溶解性规律、酸与盐的化学性质是正确解答本题关健.


科目:初中化学 来源: 题型:实验探究题
| 操作步骤 | 实验现象 | 实验结论 |
| 分别用A,B,C三支试管取样,然后各加入适量碳酸钠溶液 | A中无明显现象 B中产生气泡 C中产生沉淀 | A中的物质是食盐水 B中的物质是稀盐酸 C中的物质是澄清石灰水 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
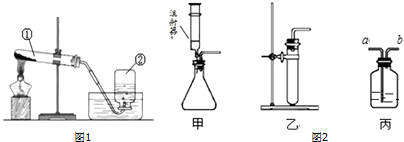
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
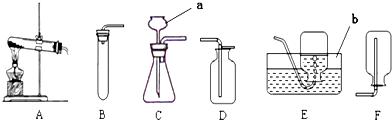
查看答案和解析>>
科目:初中化学 来源: 题型:推断题
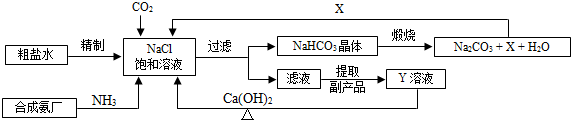
| OH- | SO42- | CO32- | |
| Mg2+ | 不 | 溶 | 微 |
| Ca2+ | 微 | 微 | 不 |
| Ba2+ | 溶 | 不 | 不 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 实验室制取氧气时,一定要用催化剂 | |
| B. | 细铁丝在氧气中可剧烈燃烧,火星四射 | |
| C. | 油锅着火,可用锅盖盖灭,依据的灭火原理是隔绝氧气 | |
| D. | 氧气能与大多数的金属、某些化合物反应,化学性质比较活泼 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com