
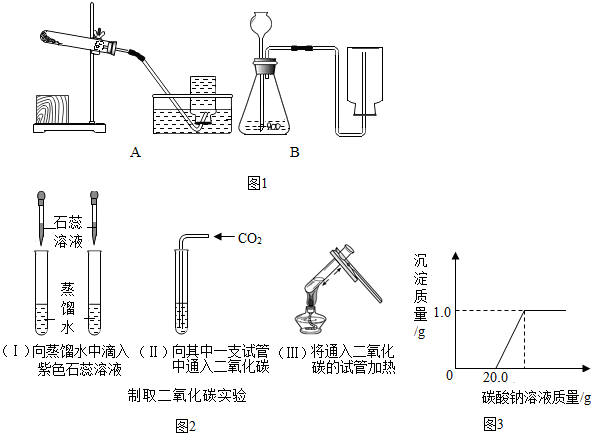
分析 (1)根据反应原理和反应条件来选择反应需要的仪器,并完成化学方程式的书写;
(2)二氧化碳的密度比空气大,应用向上排空气法收集,并据反应原理书写方程式;
(3)产生沉淀前消耗20.0g碳酸钠溶液,这是与废液中盐酸反应的碳酸钠溶液的质量,由于盐酸反应的碳酸钠溶液的质量和质量分数,根据二者反应的化学方程式可以计算出生成氯化钠和二氧化碳的质量.
由两种反应生成的氯化钠的质量和除以所得溶液的质量就得到所得溶液中氯化钠的质量分数.
解答 解:(1)高锰酸钾在加热的条件下可以分解产生二氧化锰、锰酸钾和氧气,化学方程式为:2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑,该反应需要加热,故填:酒精灯;2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑;
(2)二氧化碳的密度比空气大,应用向上排空气法收集,不能用向下排空气法收集,所以应将集气瓶正放;碳酸钙和盐酸反应生成氯化钙、水和二氧化碳,方程式是:CaCO3+2HCl═CaCl2+CO2↑+H2O,故填:应使用向上排空气法收集;CaCO3+2HCl═CaCl2+H2O+CO2↑;
(4)①设与盐酸反应时,生成氯化钠的质量为x,生成二氧化碳的质量为y.
Na2CO3+2HCl═2NaCl+CO2↑+H2O
106 117 44
20.0g×5.3% x y
$\frac{106}{117}=\frac{20.0g×5.3%}{x}$
x=1.17g
$\frac{106}{44}=\frac{20.0g}{y}$
y=0.44g
②设与氯化钙反应时,需要碳酸钠溶液的质量为z,生成氯化钠的质量为w.
Na2CO3+CaCl2═CaCO3↓+2NaCl
106 100 117
z•5.3% 1g w
$\frac{106}{z×5.3%}=\frac{100}{1g}=\frac{117}{w}$
z=20.0g
w=1.17g
实际参加反应的碳酸钠溶液的质量为
20.0g+20.0g=40.0g
所得溶液中氯化钠的质量分数为$\frac{1.17g+1.17g}{20.0g+40.0g-1g-0.44g\\;}$×100%≈4.0%
答:生成二氧化碳0.44g.所得溶液中氯化钠的质量分数为4.0%
点评 本题主要考查含杂质物质的化学方程式计算和溶质质量分数的计算,难度较大.


 小学教材全测系列答案
小学教材全测系列答案 小学数学口算题卡脱口而出系列答案
小学数学口算题卡脱口而出系列答案科目:初中化学 来源: 题型:填空题
| MnO2与KClO3的质量比 | 1:40 | 1:20 | 1:10 | 1:5 | 1:3 | 1:2 | 2:3 | 1:1 | 2:1 |
| 生成1LO2所需的时间(s) | 124 | 79 | 50 | 54 | 75 | 93 | 106 | 153 | 240 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
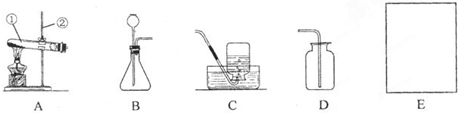
| A. | ①⑤⑦ | B. | ①③⑤⑦ | C. | ②③④⑥ | D. | ①⑤⑥⑦ |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 加入氧化铜 | B. | 加入硫酸钠 | C. | 加入石灰石(CaCO3) | D. | 加入生石灰(CaO) |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 酒精中氢元素的质量分数最大 | |
| B. | 酒精中碳、氢元素的质量比为1:3 | |
| C. | 酒精属于化合物 | |
| D. | 酒精是由2个碳原子、6个氢原子和1个氧原子构成的 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com