


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:初中化学 来源: 题型:
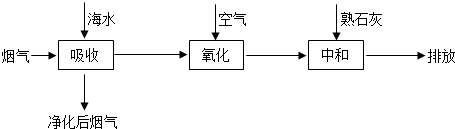
| 实验序号 | 温度/℃ | 烟气中SO2浓度/10-2g?L-1 | 脱硫率/% |
| I | 23 | 2.5% | 99.5 |
| II | 23 | 3.2% | 97.1 |
| III | 40 | 2.5% | 94.3 |
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:

| 金属 | 铁 | 铜 |
| 与盐酸反应现象 | 放出气泡 | 无明显现象 |
| 结论 | 活动性: | |
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
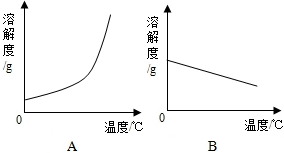 下表是Ca(OH)2 和NaOH的溶解度数据.请回答下列问题:
下表是Ca(OH)2 和NaOH的溶解度数据.请回答下列问题:| 温度/℃ | 0 | 20 | 40 | 60 | 80 | 100 | |
| 溶解度(g) | Ca(OH)2 | 0.19 | 0.17 | 0.14 | 0.12 | 0.09 | 0.08 |
| NaOH | 31 | 91 | 111 | 129 | 313 | 336 | |
查看答案和解析>>
科目:初中化学 来源: 题型:
| 反应物I | 反应物Ⅱ | 反应现象 | 说 明 |
| AgNO3溶液 | NaCl溶液 | 生成白色沉淀 | 该沉淀为AgCl,不溶于稀H NO3 |
| BaCl2溶液 | Na2SO4溶液 | 生成白色沉淀 | 该沉淀为BaSO4,不溶于稀HCl |
| Na2CO3溶液 | 生成白色沉淀 | 该沉淀为 |
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com