
将一定质量的高锰酸钾放在试管内加热一段时间后,测得反应后生成氧气的质量小于原高锰酸钾质量的10%,则反应后的固体物质与原高锰酸钾的质量比可能是
A.71︰75 B.71︰79 C.80︰79 D.81︰79
A
【解析】
试题分析:解:设原有高锰酸钾的质量为x,生成氧气的质量是高锰酸钾质量的10%,即0.1x,剩余固体质量为y。
2KMnO4 【K2MnO4+MnO2】+O2↑
【K2MnO4+MnO2】+O2↑
316 284 32
M N 0.1x
反应掉的高锰酸钾质量为M=(316×0.1x)/32
反应后剩余固体质量为N=(284×0.1x)/32
反应后的固体物质与原高锰酸钾的质量比[(284×0.1x)/32]:[(316×0.1x)/32]=71:79,但题中说明生成的氧气质量小于高锰酸钾的10%,高锰酸钾分解的更少,即生成固体质量小,两者的比值小于71:79,选A。
考点:质量守恒定律及其应用。
点评:这是一道估算类题目,根据质量守恒定律,先预设反应生成的氧气质量是原高锰酸钾质量的10%,这是解题的关键。


科目:初中化学 来源: 题型:
| A、71:75 | B、71:79 | C、80:79 | D、81:79 |
查看答案和解析>>
科目:初中化学 来源: 题型:
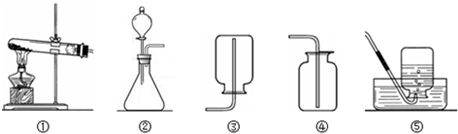
| ||
| ||
查看答案和解析>>
科目:初中化学 来源:2012年甘肃省定西市中考化学模拟试卷(八)(解析版) 题型:选择题
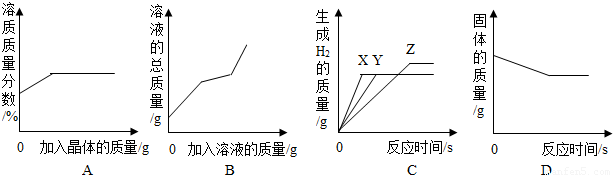
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com