
(5分)化学中质量守恒定律是一个非常重要的定量定律。
(1)右图为托盘天平,使用托盘天平称物品的正确操作顺序为(填序号) 。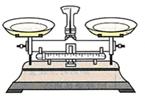
①调游码 ②放称量纸 ③称量物放左盘
④调零点 ⑤加质量大的砝码 ⑥加质量小的砝码
A.①②③④⑤⑥ B.④②③⑤⑥① C.④⑤⑥①②③
(2)如右图装置中,称量小烧杯中所有物质的质量m1,然后将小烧杯中的碳酸钠与盐酸完全混合,反应发生一段时间后,再称量小烧杯及烧瓶内物质的总质量为 m2,则(填“=”“>”“<”)m1_ _m2,其原因为 。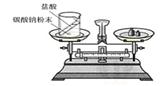
(3)化学反应前后,一定不变的是 (填数字序号)。
①原子种类 ②原子数目 ③分子种类
④分子数目 ⑤元素种类 ⑥物质总质量
(4)硝酸在工业生产中有广泛的应用,工业上制取硝酸的关键反应为: ,其中R的化学式为 。
,其中R的化学式为 。
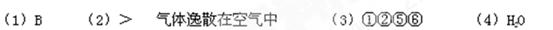
解析(1)在使用天平时必须先将游码归零,再在托盘上放上一张大小相等的纸片,然后调节平衡螺母使天平平衡,称量时注意是左物右码,加砝码的按从大到小的顺序添加;分析题给的选项可以知道正确的操作顺序为:④②③⑤⑥①,故选B;
(2)(2)盐酸和碳酸钠反应生成二氧化碳气体,而该图中的装置为敞口的装置,所以生成的二氧化碳气体要逸散到空气中,从而使烧杯中物质质量减少,即反应前的质量要大于反应后的质量,即m1>m2.
(3)(3)根据化学反应的实质,可以知道在反应前后,元素的种类、原子的种类、数目和质量不变,所以物质的总质量不变,而反应前后产生了新的物质,所以分子的种类要发生改变,分析题中的选项可以知道在反应前后不变的量为:①②⑤⑥;
(4)分析 可以知道:反应前比反应后多了12个氢原子和6个氧原子,所以在6R中含有12个氢原子和6个氧原子,那么在R中含有2个氢原子和1个氧原子,即R的化学式为:H20.
可以知道:反应前比反应后多了12个氢原子和6个氧原子,所以在6R中含有12个氢原子和6个氧原子,那么在R中含有2个氢原子和1个氧原子,即R的化学式为:H20.


科目:初中化学 来源: 题型:阅读理解
| 序号 | 反应前A的质量 | 反应前B的质量 | 反应后A3B2的质量 |
| ① | 8g | 2g | 6g |
| ② | 4g | 6g | 6g |
| ③ | xg | yg | 9g |
查看答案和解析>>
科目:初中化学 来源: 题型:
 化学中质量守恒定律是一个非常重要的定量定律.右图为托盘天平,使用托盘天平称物品的正确操作顺序为(填序号)
化学中质量守恒定律是一个非常重要的定量定律.右图为托盘天平,使用托盘天平称物品的正确操作顺序为(填序号)查看答案和解析>>
科目:初中化学 来源: 题型:
 化学中质量守恒定律是一个非常重要的定量定律.
化学中质量守恒定律是一个非常重要的定量定律.
| ||
| △ |
查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解
 化学中质量守恒定律是一个非常重要的定量定律。
化学中质量守恒定律是一个非常重要的定量定律。
(1)如右图装置中,称量小烧杯中所有物质的质量m1,然
后将小烧杯中的碳酸钠与盐酸完全混合,反应发生一
段时间后,再称量小烧杯及烧瓶内物质的总质量为
m2,则(填“=” “>”“<”)m1 m2 ,其原
因为 。
(2)天然气的主要成分是甲烷(CH4),可直接用作气体燃
料。燃烧反应前后分子种类变化的微观示意图如下所示。

①1个B分子中含有 个原子。
②四种物质中属于化合物的是 (填图中字母)。
(3)A和B可发生如下反应:3A+2B=A3B2,某学生做了3次该实验(每次均充分反应),反应前A和B的质量 和都是l0g。有关实验数据见下表:
序号 反应前A的质量 反应前B的质量 反应后A3B2的质量
① 8g 2g 6g
② 4g 6g 6g
③ xg yg 9g
X∶Y的比值可能为 或 。
(4)为了测定某品牌食用纯碱中碳酸钠的质量分数,某校化学研究性学习小组的探究过程如下:
【提出问题】样品中碳酸钠的质量分数是多少?
【知识准备】食用纯碱的主要成分是碳酸钠,另外还含有少量的氯化钠;反应过程中不考虑水和氯化氢的挥发。
【设计方案】(1)方案一:向一定量样品中加入过量澄清石灰水,根据反应生成碳酸钙的质量,先求出碳酸钠的质量,再计算样品中碳酸钠的质量分数。
(2)方案二:向一定量样品中加入足量的稀盐酸,根据反应生成二氧化碳的质量,先求出碳酸钠的质量,再计算样品中碳酸钠的质量分数。
【进行实验】甲组同学:称取24.00g样品,加水配成溶液,在溶液中加入过量的澄清石灰水。过滤、洗涤、干燥,共得到白色沉淀20.00g。
乙组同学:称取24.00g样品,加入足量的稀盐酸直到反应停止,共收集到8.80g二氧化碳。
【解决问题】请你任选一组同学的实验结果,帮助他们计算出样品中碳酸钠的质量分数。(写出计算过程。计算结果精确到0.1% )
查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解
化学中质量守恒定律是一个非常重要的定量定律。
(1)如右图装置中,称量小烧杯中所有物质的质量m1,然后将小烧杯中的碳酸钠与盐酸完全混合,反应发生一段时间后,再称量小烧杯及烧瓶内物质的总质量为 m2,则(填“=” “>”“<”)m1 m2 ,其原因为 。

(2)天然气的主要成分是甲烷(CH4),可直接用作气体燃
料。燃烧反应前后分子种类变化的微观示意图如下所示。

①1个B分子中含有 个原子。
②四种物质中属于化合物的是 (填图中字母)。
(3)A和B可发生如下反应:3A+2B=A3B2,某学生做了3次该实验(每次均充分反应),反应前A和B的质量![]() 和都是l0g。有关实验数据见下表:
和都是l0g。有关实验数据见下表:
| 序号 | 反应前A的质量 | 反应前B的质量 | 反应后A3B2的质量 |
| ① | 8g | 2g | 6g |
| ② | 4g | 6g | 6g |
| ③ | xg | yg | 9g |
X∶Y的比值可能为 或 。
(4)为了测定某品牌食用纯碱中碳酸钠的质量分数,某校化学研究性学习小组的探究过程如
下:
【提出问题】样品中碳酸钠的质量分数是多少?
【知识准备】食用纯碱的主要成分是碳酸钠,另外还含有少量的氯化钠;反应过程中不考虑水和氯化氢的挥发。
【设计方案】(1)方案一:向一定量样品中加入过量澄清石灰水,根据反应生成碳酸钙的质量,先求出碳酸钠的质量,再计算样品中碳酸钠的质量分数。
(2)方案二:向一定量样品中加入足量的稀盐酸,根据反应生成二氧化碳的质量,先求出碳酸钠的质量,再计算样品中碳酸钠的质量分数。
【进行实验】甲组同学:称取24.00g样品,加水配成溶液,在溶液中加入过量的澄清石灰水。过滤、洗涤、干燥,共得到白色沉淀20.00g。
乙组同学:称取24.00g样品,加入足量的稀盐酸直到反应停止,共收集到8.80g二氧化碳。
【解决问题】请你任选一组同学的实验结果,帮助他们计算出样品中碳酸钠的质量分数。(写出计算过程。计算结果精确到0.1% )
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com