
分析 (1)配制溶液时,首先要计算配制时所需要的溶质和溶剂的量;溶质质量=溶液质量×溶液中溶质的质量分数;溶剂质量=溶液质量-溶质质量;
(2)根据计算结果,使用天平称取固体氯化钠,并倒入烧杯;
(3)使用量量筒量取水,倒入烧杯,用玻璃棒搅拌,加快固体氯化钠的溶解.
解答 解:(1)计算所需要溶质和溶剂的量:配制100g15%的食盐水需要氯化钠的质量=100g×15%=15g,
需要水的质量=100g-15g=85g(合85mL)
(2)称量,用托盘天平称取所需的氯化钠,(其中左物氯化钠)放入烧杯中.量取水并进行溶解,根据量程相近的原则,选用100mL量筒量取所需的水;
(3)溶解:将用量筒量取的水,倒入盛有氯化钠的烧杯中,用玻璃棒搅拌.(搅拌的作用加速溶解)待氯化钠完全溶解时,15%的氯化钠溶液就配制好了.
故答案为:
(1)15;85;
(2)氯化钠;100mL;
(3)加速溶解.
点评 熟悉溶质质量分数的计算公式,浓溶液配制稀溶液的计算方法等知识,就能正确解答,难度不大.


 全能测控一本好卷系列答案
全能测控一本好卷系列答案科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | ①多 | B. | ②多 | C. | 一样多 | D. | 无法判断 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
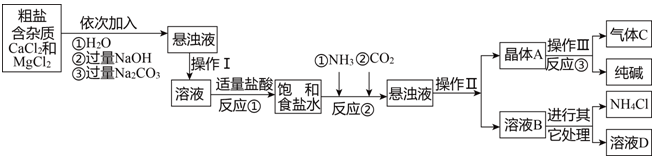
| 物质 | NaCl | NaHCO3 | NH4Cl | NH3 | CO2 |
| 溶解度 | 36.0g | 9.6g | 37.2g | 710g | 0.9g |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 溶液的总质量保持不变 | B. | 溶液中溶剂的质量保持不变 | ||
| C. | 还能继续溶解硝酸钾晶体 | D. | 剩余溶液一定是不饱和溶液 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
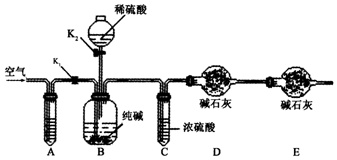
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
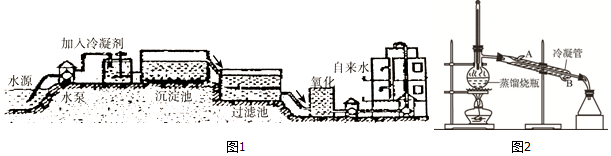
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com