
 如图所示为初中化学几种常见物质及其转化关系,请根据图示回答:
如图所示为初中化学几种常见物质及其转化关系,请根据图示回答:分析 单质A和化合物甲反应生成金属单质B和化合物乙,我们可以判断出它们发生都是还原反应,那么单质A表现出的就是还原性,而具有还原性的单质我们所学过就只有单质碳和氢气,那么化合物甲就是金属氧化物,而D就应该是氧气,化合物乙就可能是水或者是二氧化碳,分析至此可以完成解答.
解答 解:(1)根据金属单质B和单质D反应生成化合物甲,我们可以判断出甲应该是有两种元素组成的金属氧化物,故本题答案为:2;
(2)单质A和化合物甲反应生成乙和B,可知它们是还原反应,而我们常见的还原反应就是单质碳或者是氢气与氧化铜的反应,故金属B可能是铜,那么化合物乙就可能是二氧化碳或是水,故本题答案为:铜(或铁等); CO2(或H2O等);
(3)单质A和化合物甲反应生成金属单质B和化合物乙,因此该反应是置换反应;故填:置换.
点评 本题为框图式物质推断题,完成此题,可以依据框图提供的信息结合物质的性质进行.


科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | ①②③ | B. | ①③ | C. | ②③ | D. | ①② |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
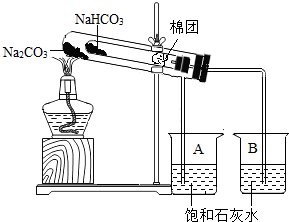 某校化学兴趣小组对苏打(Na2CO3)和小苏打(NaHCO3)在生活中具有何作用,如何鉴别苏打和小苏打进行了如下的探究实验活动,请你参与他们的探究过程,并回答相关问题:
某校化学兴趣小组对苏打(Na2CO3)和小苏打(NaHCO3)在生活中具有何作用,如何鉴别苏打和小苏打进行了如下的探究实验活动,请你参与他们的探究过程,并回答相关问题:查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 如图所示,打开分液漏斗,使其中的无色液体与烧瓶中的固体接触反应,可观察到尖嘴导管口处有水喷出,请分别写出一个符合图中现象和下列要求的化学方程式:
如图所示,打开分液漏斗,使其中的无色液体与烧瓶中的固体接触反应,可观察到尖嘴导管口处有水喷出,请分别写出一个符合图中现象和下列要求的化学方程式:查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 水是一种氧化物 | B. | 水是生命活动中不可缺少的物质 | ||
| C. | 水由氢分子和氧原子构成 | D. | 电解水时在负极得到氢气 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com