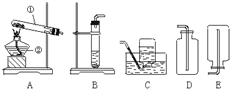
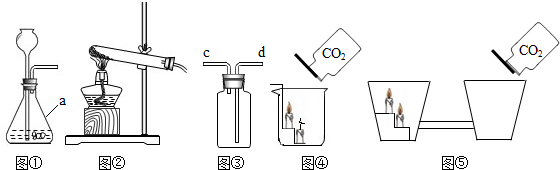
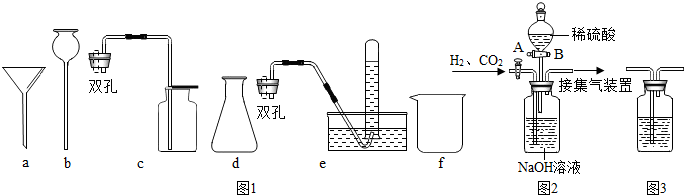
下面是实验室制取氧气的装置图,根据装置图回答下列问题:
(1)写出装置图中标有①②序号的仪器名称:①
试管
试管
;②
酒精灯
酒精灯
.
(2)实验室用氯酸钾制取氧气时的化学表达式
,可选用的发生装置是
A
A
;可选用的收集装置是
C
C
和
D
D
.
(3)装置B是实验室用
过氧化氢
过氧化氢
和
二氧化锰
二氧化锰
制取氧气的发生装置.
(4)用加热高锰酸钾制取氧气时,常在试管口放一团
防止高锰酸钾粉末进入导管
防止高锰酸钾粉末进入导管
,反应的化学表达式为
.
(5)用D装置收集氧气的依据是
氧气的密度略大于空气的密度
氧气的密度略大于空气的密度
,用该方法收集氧气时,检验氧气是否集满的方法是
将带火星的木条伸入瓶口处,若木条复燃,则证明氧气收集满了
将带火星的木条伸入瓶口处,若木条复燃,则证明氧气收集满了
.
(6)实验室常用氯化铵固体与碱石灰固体共热来制取氨气.常温下NH
3是一种无色、有刺激性气味的气体,密度比空气小.NH
3极易溶于水,其水溶液呈碱性.实验室制取并收集NH
3,应该从上图中选择的装置是
AE
AE
.
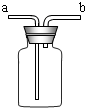
(7)若用如图所示装置有多种用途,①收集氨气时,氨气应从
b
b
管口通入瓶中;②若将瓶中装满水,收集氢气或氧气时,气体应从
b
b
管口通入瓶中;③若将瓶中装入半瓶蒸馏水可用于病人输送装置,
a
a
端连接贮氧气钢瓶,在输送的过程中,这一装置能起到的作用是
观察是否有氧气输出
观察是否有氧气输出
、
观察氧气的流速
观察氧气的流速
、
湿润氧气
湿润氧气
.
[拓展探究]
学校化学兴趣小组的同学知道二氧化锰能作过氧化氢(H
2O
2)分解的催化剂后,想再探究其他一些物质如Al
2O
3是否也可作过氧化氢分解的催化剂.请你一起参与他们的探究过程,并填写下列空白.
[提出问题]Al
2O
3能不能作过氧化氢分解的催化剂呢?
[作出猜想]Al
2O
3能作过氧化氢分解的催化剂.
[实验验证]
|
实验步骤 |
实验现象 |
实验结论 |
| 实验一 |
将带火星的木条伸入装有过氧化氢溶液的试管中 将带火星的木条伸入装有过氧化氢溶液的试管中 |
有少量气泡
木条不复燃 |
常温下过氧化氢溶液分解速率很慢. |
| 实验二 |
在装有过氧化氢溶液的试管中加入少量Al2O3,然后将带火星的木条伸入试管中 |
产生大量的气泡木条复燃 |
加入Al2O3能加快过氧化氢溶液的分解速率 加入Al2O3能加快过氧化氢溶液的分解速率 |
[得出结论]Al
2O
3能加快过氧化氢的分解速率,故Al
2O
3能作过氧化氢分解的催化剂.
[反思提高]经过讨论,有的同学认为只有上述两个证据,不能证明Al
2O
3能作过氧化氢分解的催化剂,还要补充一个探究实验:
实验三:
[实验目的]探究
Al2O3在反应前后质量是否改变
Al2O3在反应前后质量是否改变
.
[实验步骤]①准确称量Al
2O
3(少量)的质量;②完成实验二;③待反应结束,将实验二试管里的物质进行过滤,洗涤,
干燥
干燥
,称量;④对比反应前后Al
2O
3的质量.
[交流讨论]如果Al
2O
3在反应前后质量不变,则说明Al
2O
3可以作过氧化氢分解的催化剂.
[提出新的问题]但小华认为,要证明猜想,上述三个实验还不足够,还需要再增加一个探究实验:探究
Al2O3的化学性质在反应前后是否改变
Al2O3的化学性质在反应前后是否改变
.



 学而优衔接教材南京大学出版社系列答案
学而优衔接教材南京大学出版社系列答案

 下面是实验室制取氧气的装置图,根据装置图回答下列问题:
下面是实验室制取氧气的装置图,根据装置图回答下列问题: