

 ______.要得到科学严谨的结论,仍利用该装置,补做的实验是______.
______.要得到科学严谨的结论,仍利用该装置,补做的实验是______.| 实验过程 | 实验现象 | 实验结论 |
| 在一支试管中加入5ml5%的H2O2溶液,然后滴入适量的FeCl3溶液,把带火星的木条伸入试管. | ______ | FeCl3溶液可以催化分解H2O2 |
| 实验过程 | 实验现象 | 实验结论 |
| 向盛有5ml5%的H2O2溶液的试管中加入少量的HCl,并把带火星的木条伸入试管 | 无明显现象 | ______ |
| 向盛有5ml5%的H2O2溶液的试管中加入少量的______,并把带火星的木条伸入试管 | ______ | ______ |
| 实验步骤 | 实验现象 | 结论 |
| 起催化作用的不是Cl- | ||
| Fe(NO3)3溶液 | 试管中有大量气泡产生,带火星的木条复燃 | 起催化作用的是Fe3+ |
| 实验步骤 | 实验现象 | 结论 |
| 起催化作用的不是Cl- | ||
| Fe(NO3)3溶液 | 试管中有大量气泡产生,带火星的木条复燃 | 起催化作用的是Fe3+ |


 开心蛙口算题卡系列答案
开心蛙口算题卡系列答案科目:初中化学 来源: 题型:
| 猜想 | 实验步骤 | 现象 | 结论 |
| 猜想① | 将上述红色溶液分成两份,在一份中加少量的植物油. | 没加植物油的红色褪去,另一红色没褪去 |
若猜想①成立 |
| 猜想② | 将上述红色溶液分成两份,并用植物油封住, 一支温度保持不变,另一支自然冷却 . |
前者红色没褪去,后者红色褪去 |
猜想②成立 |
查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解
 23、请你参与下列探究:
23、请你参与下列探究:查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解
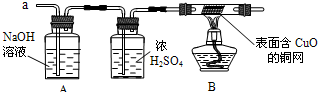
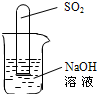
| 实验过程 | 实验现象 | 实验结论 |
| 在一支试管中加入5ml5%的H2O2溶液,然后滴入适量的FeCl3溶液,把带火星的木条伸入试管. | 试管中有大量的气泡产生,伸入的带火星的木条复燃 |
FeCl3溶液可以催化分解H2O2 |
| 实验过程 | 实验现象 | 实验结论 |
| 向盛有5ml5%的H2O2溶液的试管中加入少量的HCl,并把带火星的木条伸入试管 | 无明显现象 | 起催化作用的不是Cl- |
| 向盛有5ml5%的H2O2溶液的试管中加入少量的 Fe(NO3)3溶液 ,并把带火星的木条伸入试管 |
试管中有大量气泡产生,带火星的木条复燃 |
起催化作用的是Fe3+ |
查看答案和解析>>
科目:初中化学 来源: 题型:

查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解
| ||
| ||
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com