B
分析:氢氧化钠溶液显碱性,碱性溶液的pH大于7;向NaOH溶液中不断滴加盐酸溶液时,盐酸与氢氧化钠发生中和反应生成氯化钠和水,氯化钠溶液呈中性,中性溶液的pH等于7;由于氢氧化钠减少,所以溶液的pH不断减小,当盐酸与氢氧化钠恰好完全发生时,溶液呈中性,溶液的pH等于7;再滴加稀盐酸,溶液显酸性,溶液的pH小于7.
解答:
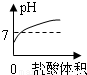
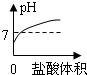
A、由于氢氧化钠溶液显碱性,碱性溶液的pH大于7,所以图象上的起点不应在7下方,故A错误;
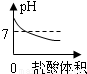
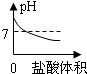
B、氢氧化钠溶液显碱性,碱性溶液的pH大于7;向NaOH溶液中不断滴加盐酸溶液时,盐酸与氢氧化钠发生中和反应生成氯化钠和水,氯化钠溶液呈中性,中性溶液的pH等于7;
由于氢氧化钠减少,所以溶液的pH不断减小,当盐酸与氢氧化钠恰好完全发生时,溶液呈中性,溶液的pH等于7;再滴加稀盐酸,溶液显酸性,溶液的pH小于7;故B正确
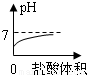
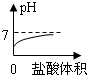
C、由于氢氧化钠溶液显碱性,碱性溶液的pH大于7,所以图象上的起点不应在7下方,而且因为最终加入的盐酸过量时,溶液显酸性,所以终点应在7的下方,故C错误;
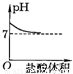
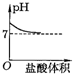
D、因为当最终加入的盐酸过量时,溶液显酸性,所以终点应在7的下方,故D错误;
故选B
点评:这是一道函数图象的考题,重点考查了酸和碱的pH以及酸碱中和的问题,是考试的重点.



 互动英语系列答案
互动英语系列答案 名牌学校分层周周测系列答案
名牌学校分层周周测系列答案