解:(1)根据常用仪器名称和用途可知这些仪器分别是:烧杯、试管、长颈漏斗、酒精灯;
故答案为:A、烧杯 B、试管 D、长颈漏斗 H、酒精灯;
(2)高锰酸钾在加热的条件下生成锰酸钾、二氧化锰和氧气,方程式是2KMnO
4
K
2MnO
4+MnO
2+O
2↑,实验时需用试管装药品,铁架台固定试管,加热要用酒精灯,排水法收集还需要集气瓶和水槽;
故答案为:B、C、E、G、H;2KMnO
4
K
2MnO
4+MnO
2+O
2↑;
(3)过氧化氢在二氧化锰作催化剂的条件下生成水和氧气,方程式是2H
2O
2
2H
2O+O
2↑,实验时用试管或锥形瓶装药品,要随时添加过氧化氢,还需选择长颈漏斗,一般制取少量氧气用试管,制取较多氧气用锥形瓶;
故答案为:2H
2O
2
2H
2O+O
2↑;B、D、E(或F、D).
(4)NH
4Cl和固体Ca(OH)
2加热制得NH
3,同时得到氯化钙和水,反应的方程式是2NH
4Cl+Ca(OH)
2
CaCl
2+2H
2O+2NH
3↑,配平时以氯化铵中的氯原子为起点进行配平,再配平氮原子、氧原子,最后配平氢原子;实验时用试管装药品,铁架台固定,酒精灯加热,氨气能溶于水,不能用排水法收集,故不选水槽;
故答案为:2NH
4Cl+Ca(OH)
2
CaCl
2+2H
2O+2NH
3↑;B、C、E、H;
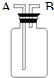
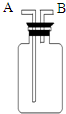
(5)氧气的密度比空气大,所以用排空气法收集时,要从长导管进入,便于排尽空气,氧气的密度比水小,所以用排水法收集时要从短导管进入,长导管排水,更易排尽;
故答案为:A、B.
分析:(1)根据常用仪器名称和用途判断;
(2)根据高锰酸钾制取氧气的反应原理和氧气的性质确定所用仪器,并书写化学方程式;
(3)根据过氧化氢制取氧气的反应原理书写化学方程式,并确定所用仪器,要随时添加药品,需选择长颈漏斗;
(4)根据反应物、生成物和反应条件书写化学方程式,并依据反应原理和氨气的性质选择仪器;
(5)氧气的密度比空气大,所以用排空气法收集时应从长导管进气,便于排尽空气,用排水法收集时,从短导管进气,长导管出水,更易将水排尽.
点评:本题主要考查了实验室制取气体仪器的选取,方程式的书写,明确装置的选取方法和化学反应原理及方程式书写方法是解答的关键.

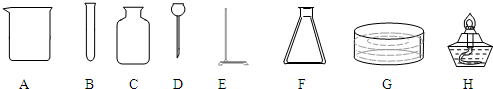
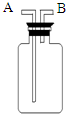 O2由______口进入;若在装置中充满水,则O2应由______口进入(填编号).
O2由______口进入;若在装置中充满水,则O2应由______口进入(填编号). K2MnO4+MnO2+O2↑,实验时需用试管装药品,铁架台固定试管,加热要用酒精灯,排水法收集还需要集气瓶和水槽;
K2MnO4+MnO2+O2↑,实验时需用试管装药品,铁架台固定试管,加热要用酒精灯,排水法收集还需要集气瓶和水槽; K2MnO4+MnO2+O2↑;
K2MnO4+MnO2+O2↑; 2H2O+O2↑,实验时用试管或锥形瓶装药品,要随时添加过氧化氢,还需选择长颈漏斗,一般制取少量氧气用试管,制取较多氧气用锥形瓶;
2H2O+O2↑,实验时用试管或锥形瓶装药品,要随时添加过氧化氢,还需选择长颈漏斗,一般制取少量氧气用试管,制取较多氧气用锥形瓶; 2H2O+O2↑;B、D、E(或F、D).
2H2O+O2↑;B、D、E(或F、D). CaCl2+2H2O+2NH3↑,配平时以氯化铵中的氯原子为起点进行配平,再配平氮原子、氧原子,最后配平氢原子;实验时用试管装药品,铁架台固定,酒精灯加热,氨气能溶于水,不能用排水法收集,故不选水槽;
CaCl2+2H2O+2NH3↑,配平时以氯化铵中的氯原子为起点进行配平,再配平氮原子、氧原子,最后配平氢原子;实验时用试管装药品,铁架台固定,酒精灯加热,氨气能溶于水,不能用排水法收集,故不选水槽; CaCl2+2H2O+2NH3↑;B、C、E、H;
CaCl2+2H2O+2NH3↑;B、C、E、H;


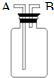
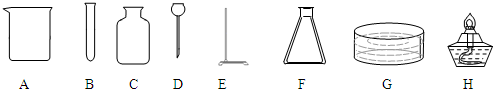
 O2由
O2由