
 某化学兴趣小组的小军等几位同学进行了如下图所示的实验:鉴别碳酸钠溶液和氢氧化钠溶液,
某化学兴趣小组的小军等几位同学进行了如下图所示的实验:鉴别碳酸钠溶液和氢氧化钠溶液,| 实验步骤 | 实验现象 | 实验结论 |
| 取样于试管中,滴入适量的稀盐酸 | 有气泡产生 | 你的猜想是正确 |
分析 (1)根据碳酸钠与氢氧化钙反应生成碳酸钙沉淀和氢氧化钠解答;
(2)氧化钙和碳酸钠溶液反应时,存在物质过量的问题,可能是氢氧化钙过量,可能是氢氧化钠过量进行猜想解答;
根据碳酸钠溶液遇盐酸反应生成二氧化碳气体解答.
解答 解:(1)氢氧化钙能与碳酸钠反应生成碳酸钙沉淀和氢氧化钠,故填:Ca(OH)2+Na2CO3=CaCO3↓+2NaOH;
(2)猜想:氢氧化钙和碳酸钠溶液反应时,存在物质过量的问题,可能是氢氧化钙过量,可能是氢氧化钠过量,由于反应生成氢氧化钠,故可能是氢氧化钠和碳酸钠的混合物;
实验设计:要证明碳酸钠存在,可以向样品中滴入适量的稀盐酸,如果试管中有气泡产生,说明是碳酸钠和氢氧化钠的混合物.
答案:
(1)Na2CO3+Ca(OH)2═2NaOH+CaCO3↓;
(2)氢氧化钠和碳酸钠;滴入适量的稀盐酸(符合题意的均可);有气泡产生.
点评 本题考查了常见物质变质成分的探究,完成此题,可以依据物质的性质进行.要求同学们熟练掌握常见物质的性质,以便灵活应用.


科目:初中化学 来源: 题型:推断题
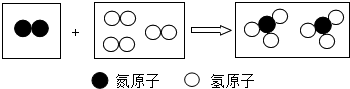 如图是某反应的微观过程.
如图是某反应的微观过程.查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | pH:酸雨>正常雨水 | |
| B. | 常温条件下在水中的溶解性:氢氧化钙>氢氧化钠 | |
| C. | 溶于水后溶液的温度:氢氧化钠>硝酸铵 | |
| D. | 所有原子中:质子数>核外电子数 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 冬天用煤炉取暖,为防止热量散失,应关紧门窗 | |
| B. | 进入干涸的深井前,应先做灯火试验 | |
| C. | 用NaHCO3治疗胃酸过多 | |
| D. | 铵态氮肥与熟石灰混合使用会降低肥效 |
查看答案和解析>>
科目:初中化学 来源: 题型:推断题
 A、B、C、D、E是初中化学常见的不同类别物质(单质、氧化物、酸、碱和盐),它们之间相互关系如图(“→”表示反应转化关系,“-”表示相互之间能反应,部分反应物、生成物以及反应条件省略).若往D、E两种溶液中分别滴入紫色石蕊试液,溶液均显蓝色;D与E两种溶液混合有白色沉淀产生;C与E的溶液反应有气泡产生,该气体能使澄清石灰水变浑浊.请回答下列问题:
A、B、C、D、E是初中化学常见的不同类别物质(单质、氧化物、酸、碱和盐),它们之间相互关系如图(“→”表示反应转化关系,“-”表示相互之间能反应,部分反应物、生成物以及反应条件省略).若往D、E两种溶液中分别滴入紫色石蕊试液,溶液均显蓝色;D与E两种溶液混合有白色沉淀产生;C与E的溶液反应有气泡产生,该气体能使澄清石灰水变浑浊.请回答下列问题:查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com