
���� �������е�֪ʶ���з�������ʯ�Ҿ��м��ԣ������ڸ�������������������þ�������ᷴӦ�����Ȼ�þ��ˮ���������ʵ����ʲ��켴�ɽ������ʵļ���
��� �⣺��1����ʯ�Ҿ��м��ԣ������ڸ������������������ʯ�ң�
��2��������þ�������ᷴӦ�����Ȼ�þ��ˮ�����Mg��OH��2+2HCl=MgCl2+2H2O���÷�Ӧ�����кͷ�Ӧ��
��3������������������ˮ������ˮ���ȵ����ʣ��Ȼ���������ˮ���������ı仯��̼��Ʋ�����ˮ��ʹ��ˮ���м���ʱ����������ˮ���ȣ�������ʵ����������ƣ����������������ˮ���ȣ�
�𰸣�
��1����ʯ�ң�
��2��Mg��OH��2+2HCl=MgCl2+2H2O���кͷ�Ӧ��
��3��������������ˮ���ȣ�
���� ���⿼���˳������ʵ���;�Լ��йػ�ѧ����ʽ����д�����ʵļ�����ɴ��⣬�����������ʵ����ʽ��У���д��Ӧ�Ļ�ѧ����ʽҪע����ƽ��


 ��ʦ����ָ���ο�ʱϵ�д�
��ʦ����ָ���ο�ʱϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ˮ�ڡ�ʱ�����������ȼ | |
| B�� | �Ѹɱ��������ʯ��ˮ�У�ȼ��ú�����γ�����Ĺ��� | |
| C�� | �˵�ˮ��δ�ɵ������⣻ʯ��ʯ������ | |
| D�� | dz��ɫ��Һ�������ɫ���������ý��ʯ�и�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ʯ�� | B�� | ���� | C�� | ľ̿ | D�� | ��˿ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 2P+5O2$\frac{\underline{\;��ȼ\;}}{\;}$P2O5 | B�� | CO+O2$\frac{\underline{\;��ȼ\;}}{\;}$2CO2�� | ||
| C�� | 2H2+O2��$\frac{\underline{\;��ȼ\;}}{\;}$2H2O | D�� | 2KMnO4$\frac{\underline{\;\;��\;\;}}{\;}$K2MnO4+MnO2+O2�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
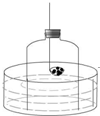 ��ͼ��ʾװ�ã�ȼ�ճ���ʢ�ŵ��Ǻ��ף�������ʵ���Ҳⶨ�����������ĺ�������ȼ�ճ��к���ȼ��Ѹ�����벣�������ڣ�������Ƥ��������ʵ������ش��������⣺
��ͼ��ʾװ�ã�ȼ�ճ���ʢ�ŵ��Ǻ��ף�������ʵ���Ҳⶨ�����������ĺ�������ȼ�ճ��к���ȼ��Ѹ�����벣�������ڣ�������Ƥ��������ʵ������ش��������⣺�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 �����Ѿ�֪������������Ҫ�ɷ��ǵ�������������ͼ�Dzⶨ������ ����������ʵ��װ�ã��Իش��������⣮
�����Ѿ�֪������������Ҫ�ɷ��ǵ�������������ͼ�Dzⶨ������ ����������ʵ��װ�ã��Իش��������⣮�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

| ʵ�� | ʵ������ | ʵ����������� |
| A | ���ҷ�Ӧ��Ѹ�ٷų��������� | ��Ӧ���ʹ��죬���岻���ռ���������ʵ������ȡ������̼ |
| B | �������ݣ�����Ѹ�ټ�������Ӧ����ֹͣ�� | ����������CO2����������ʵ������ȡCO2 |
| C | �ٲ����������� | �ڷ�Ӧ�������У���������ռ� |
| ʵ����� | H2O2�� ҺŨ��% | H2O2��Һ���/mL | �¶ȡ� | MnO2������/g | �ռ����������/mL | ��Ӧ���� ��ʱ��/s |
| �� | 5 | 1 | 20 | 0.1 | 4 | 16.75 |
| �� | 15 | 1 | 20 | 0.1 | 4 | 6.04 |
| �� | 30 | 5 | 35 | 2 | 49.21 | |
| �� | 30 | 5 | 55 | 2 | 10.76 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com