由碳、氢、氧三种元素组成的有机化合物46g,在足量的氧气中完全燃烧后,测得生成二氧化碳88g,水54g,通过计算,求出该化合物的化学式.
解:由题意可知,该物质中含碳元素为:88g×100%=24g;氢元素的质量为:54g×

×100%=6g;则所含氧元素的质量为46g-24g-6g=16g.即该化合物是由碳元素、氢和氧元素组成的.
其中碳原子:氢原子:氧原子=

:
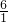
:

=2:6:1
所以该物质的化学式为:C
2H
6O
答:该化合物的化学式为C
2H
6O.
分析:根据质量守恒定律可知:生成二氧化碳中碳元素的质量等于该化合物中碳元素的质量;生成的水中氢元素的质量等于该化合物中氢元素的质量;其余则为氧元素的质量.根据该化合物的元素质量比就可以确定其的化学式.
点评:物质在氧气中完全燃烧,产物只有二氧化碳和水.根据化学反应前后元素的种类和质量都不变,则生成的二氧化碳中碳元素的质量就是物质中碳元素的质量;生成的水中氢元素的质量就是物质中氢元素的质量.若碳元素与氢元素的质量和等于物质质量,则物质中不含氧元素;若小于物质质量,则物质中含有氧元素.

 ×100%=6g;则所含氧元素的质量为46g-24g-6g=16g.即该化合物是由碳元素、氢和氧元素组成的.
×100%=6g;则所含氧元素的质量为46g-24g-6g=16g.即该化合物是由碳元素、氢和氧元素组成的. :
: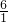 :
: =2:6:1
=2:6:1

 期末冲刺100分创新金卷完全试卷系列答案
期末冲刺100分创新金卷完全试卷系列答案