
|
| 39.6g |
| 1.9g?L-1 |


 黄冈天天练口算题卡系列答案
黄冈天天练口算题卡系列答案科目:初中化学 来源: 题型:
| 质量分数 | 0.2% | 1% | 5% | 25% |
| pH | 11.3 | 11.6 | 12.0 | 12.3 |
查看答案和解析>>
科目:初中化学 来源: 题型:
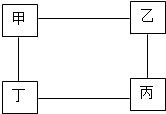 (2010?莆田)如右图所示,甲、乙、丙、丁分别为下列物质中的某一种:盐酸、硫酸、氢氧化钠和碳酸钠,图中直线相连的两种物质或其溶液都能相互发生反应.
(2010?莆田)如右图所示,甲、乙、丙、丁分别为下列物质中的某一种:盐酸、硫酸、氢氧化钠和碳酸钠,图中直线相连的两种物质或其溶液都能相互发生反应.查看答案和解析>>
科目:初中化学 来源: 题型:
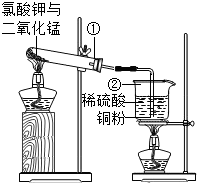 (2010?莆田)已知:2Cu+2H2SO4+O2
(2010?莆田)已知:2Cu+2H2SO4+O2
| ||
| ||
| △ |
| ||
| △ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com