(1)物质X燃烧反应的化学方程式为:X+3O2═2CO2+3H2O,由此可知X的化学式为______;
(2)一定质量的KClO3与a g MnO2的混合物加热至完全反应后,剩余固体的质量为b g,则生成KCl的质量为______g;
(3)已知一个锌原子的质量为m kg,一个作为相对原子质量计算标准的碳原子质量为n kg,则锌的相对原子质量可用含m、n的式子表示为______.
解:(1)根据反应的化学方程式X+3O
2═2CO
2+3H
2O,反应物中氧原子个数分别为6,反应后的生成物中碳、氧、氢原子个数分别为2、7、6,根据反应前后原子种类、数目不变,则每个X分子由2个碳、6个氢原子、1个氧原子构成,则物质X的化学式为C
2H
6O.
(2)一定质量的KClO
3与agMnO
2的混合物加热至完全反应后,完全反应后剩余固体为氯化钾和二氧化锰的混合物;由于该反应中二氧化锰作催化剂,反应前后质量不变,完全反应后剩余固体的质量为bg,则生成KCl的质量为b-ag.
(3)已知一个锌原子的质量为mkg,一个作为相对原子质量计算标准的碳原子质量为nkg,则锌的相对原子质量=

=
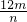
.
故答案为:(1)C
2H
6O;(2)b-a;(3)
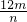
.
分析:(1)由质量守恒定律:反应前后,原子种类、数目均不变,据此由反应的化学方程式推断反应物X的化学式.
(2)根据该反应中二氧化锰作催化剂,反应前后质量不变,完全反应后剩余固体为氯化钾和二氧化锰的混合物,由完全反应后剩余固体的质量为bg计算出生成KCl的质量即可.
(3)根据某原子的相对原子相对质量=

,结合题意进行分析解答.
点评:本题难度不大,理解质量守恒定律、利用化学反应前后原子守恒来确定物质的化学式的方法、相对原子相对质量的计算方法等是正确解题的关键.

 =
=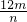 .
.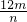 .
. ,结合题意进行分析解答.
,结合题意进行分析解答.

 字词句篇与同步作文达标系列答案
字词句篇与同步作文达标系列答案