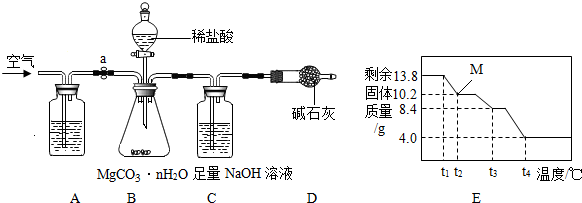
碳酸镁晶须广泛应用于冶金、耐火材料及化工产品等领域.为测定碳酸镁晶须中n的值,学习小组设计了如下装置并进行了3次实验:(不考虑稀盐酸挥发)

[查阅资料]:
a、碳酸镁晶体受热分解,生成3种氧化物;
b、相对分子质量:[Mr(MgCO
3):84、Mr(H
2O):18、Mr(MgO):40、Mr(CO
2):44]
[实验步骤]
①
;
②准确称取3.45g MgCO
3?nH
2O放在B装置中,连接仪器;
③打开弹簧夹a,鼓入一段时间空气,称量C装置的质量;
④关闭弹簧夹a,打开分液漏斗活塞,缓缓滴入稀盐酸至不再产生气体为止;
⑤打开弹簧夹a,
;
⑥准确称量C装置的质量(如表);
| 编 号 | 1 | 2 | 3 |
| 实验前 | 228.00 | 228.00 | 228.00 |
| 实验后 | 229.10 | 229.11 | 229.09 |
⑦重复上述步骤;
⑧根据数据进行计算.
[实验分析及数据处理]
(1)完善实验步骤:①
;⑤
;
(2)请计算碳酸镁晶须中的n值.(要求有计算过程,3分)
(3)A装置中盛放的溶液是
;
(4)D装置的作用是
;
[实验反思]
(5)实验结果与理论值有偏差,原因可能是
;
(6)下列选项中,会造成实验结果偏大的是
;偏小的是
;
①反应结束后,没有通空气; ②称量C装置前,没有通空气;
③没有A装置; ④没有D装置;
⑤稀盐酸滴加速率太快; ⑥C装置中NaOH溶液浓度过大;
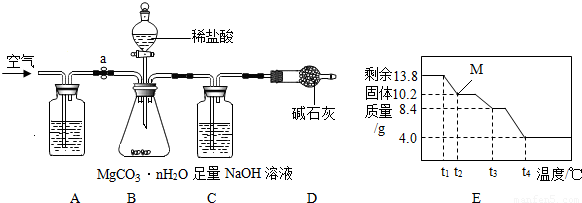
(7)为精确测定n的值,在老师指导下,小组同学称取13.8g MgCO
3?nH
2O进行热重分析,并绘制出如图所示的热重曲线示意图.则:

①t
2℃时,剩余固体为
(填化学式);
②最终剩余的4.0g物质是
(填化学式);
③MgCO
3?nH
2O完全分解的化学方程式为:
.



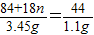
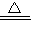 MgCO3?xH2O+(3-x)H2O
MgCO3?xH2O+(3-x)H2O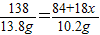
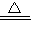 MgO+CO2↑+3H2O
MgO+CO2↑+3H2O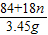 =
=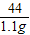
 MgO+CO2↑+3H2O
MgO+CO2↑+3H2O