(2013?江都市模拟)现有如图1下列装置,回答问题:
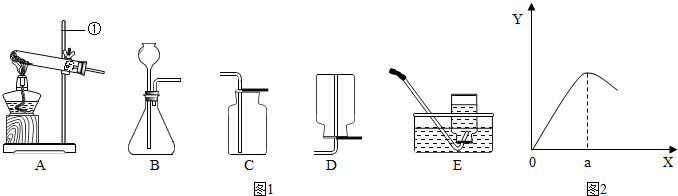
(1)写出有标号仪器的名称:①
铁架台
铁架台
;
(2)检查B装置的气密性的方法是:
用弹簧夹夹住右侧导气管
用弹簧夹夹住右侧导气管
,向长颈漏斗中加适量的水,若观察到长颈漏斗末端出现稳定的水柱,则装置不漏气;
(3)实验室制取H
2的反应化学方程式为
Zn+H2SO4═ZnSO4+H2↑
Zn+H2SO4═ZnSO4+H2↑
,发生装置为
B
B
;
(4)实验发现:用40%的硫酸制取H
2效果最好.现欲配制30mL 40%(密度为1.30g?mL
-1)的硫酸,需要98%(密度为1.84g?mL
-1)的浓硫酸
8.7
8.7
mL(精确到小数点后一位),需要水
23.0
23.0
mL(精确到小数点后一位).量取浓硫酸时,若仰视读数(其他操作均正确),则所配硫酸的质量分数
>
>
40%(填“>”或“=”或“<”),配制过程不需要的仪器是
AF
AF
;
A.托盘天平 B.量筒 C.烧杯 D.玻璃棒 E.胶头滴管 F.铁架台
(5)实验室制取H
2时,在硫酸溶液中滴入饱和CuSO
4溶液会影响反应速率.如图2是滴入饱和CuSO
4溶液体积(X)与反应速率(Y)的关系图,请回答:
①滴入CuSO
4溶液后,发生反应的化学方程式为
Zn+CuSO4═ZnSO4+Cu
Zn+CuSO4═ZnSO4+Cu
;
②a点过后,反应速率降低的原因可能是
生成的Cu覆盖在Zn表面,阻止反应进一步进行(或硫酸浓度变小,使反应速率降低)
生成的Cu覆盖在Zn表面,阻止反应进一步进行(或硫酸浓度变小,使反应速率降低)
.




 阅读快车系列答案
阅读快车系列答案