
【题目】2017年5月,中国首架无人机C919客机在浦东机场首飞成功。回答问题:
(1)选用铝合金做飞机机身而不选用纯铝,主要原因是铝合金硬度和强度_______(填“大于”或“小于”) 纯铝。铝抗腐蚀性强的原因___________(用化学方程式表示)。

(2)材料对我们的生活影响越来越大,钛合金属于_______。
A 合成材料 B 金属材料 C 复合材料 D 天然材料
(3)小军同学为了探究几种金属的性质,做了下列四个实验:
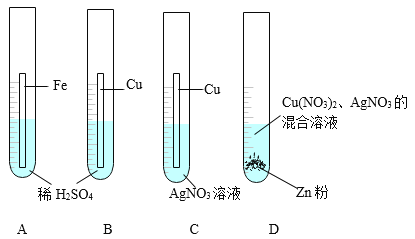
① 通过A中有气泡产生、B中__________、C中______________________的现象,可探究出Cu、Fe、Ag的金属活动性强弱为__________________。
② D中物质充分反应后过滤,滤液仍为蓝色,下列说法正确的是________(填字母)。
A 滤渣一定有银,一定没有铜和锌
B 滤渣一定有银,可能有铜,一定没有锌
C 滤液中一定有Cu2+,可能有Zn2+和Ag+
D 滤液中一定有Cu2+和Zn2+,可能有Ag+
【答案】大于 ![]() B 无明显变化 铜丝表面有银白色固体析出,溶液由无色变为蓝色 Fe>Cu> Ag BD
B 无明显变化 铜丝表面有银白色固体析出,溶液由无色变为蓝色 Fe>Cu> Ag BD
【解析】
(1)选用铝合金做飞机机身而不选用纯铝,因为合金的硬度和强度都要大于纯金属,故填大于;
铝抗腐蚀性强的原因是铝在常温下与空气中的氧气反应生成一层结构致密的氧化铝薄膜,覆盖在铝的表面,阻止铝的进一步氧化,故反应的化学方程式写为:4Al+3O2=2Al2O3。
(2)金属材料包含纯金属及合金,所以钛合金属于金属材料,故填B。
(3) ①铜位于金属活动性顺序表中氢的后面,则铜不与稀硫酸反应,观察到的现象是无明显变化,故填无明显变化;
铜的活动性位于金属活动性顺序表中银的前面,则铜与硝酸银反应生成硝酸铜和银,观察到的现象是铜丝表面有银白色固体析出,溶液由无色变为蓝色,故填铜丝表面有银白色固体析出,溶液由无色变为蓝色;
A中发生反应:Fe + H2SO4 = FeSO4 + H2↑,说明铁的活动性位于金属活动性顺序表中氢的前面, B中没有发生化学反应,无明显变化,说明铜的金属活动性位于金属活动性顺序表中氢的后面,C中发生反应Cu + 2AgNO3= 2Ag + Cu(NO3)2 ,说明铜的活动性比银强,所以三种金属活动性由强到弱的顺序为 Fe>Cu>Ag,故填Fe>Cu>Ag;
②A 将Zn粉入Cu(NO3)2、AgNO3的混合溶液中,锌先与硝酸银反应生成硝酸锌和银,待AgNO3完全反应后,Zn粉再与Cu(NO3)2溶液反应生成硝酸锌和铜,所以滤渣中一定有银,滤液仍为蓝色说明锌完全反应,则滤渣中一定没有锌,滤液仍为蓝色还说明硝酸铜没有参加反应或部分与锌发生反应,所以滤渣中可能含有铜,选项错误;
B 将Zn粉入Cu(NO3)2、AgNO3的混合溶液中,锌先与硝酸银反应生成硝酸锌和银,待AgNO3完全反应后,Zn粉再与Cu(NO3)2溶液反应生成硝酸锌和铜,所以滤渣中一定有银,滤液仍为蓝色说明锌完全反应,则滤渣中一定没有锌,滤液仍为蓝色还说明硝酸铜没有参加反应或部分与锌发生反应,所以滤渣中可能含有铜,选项正确;
C 将Zn粉入Cu(NO3)2、AgNO3的混合溶液中,锌先与硝酸银反应生成硝酸锌和银,所以滤液中一定含有硝酸锌解离出的Zn2+,滤液仍为蓝色,说明Cu(NO3)2 溶液剩余,则滤液中一定含有硝酸铜解离出的Cu2+,滤液仍为蓝色,表明可能硝酸铜没有与锌反应,则可能全部的锌只与部分硝酸银反应,所以滤液中可能有硝酸银剩余,即滤液中可能含有硝酸银解离出的Ag+,选项错误;
D 将Zn粉入Cu(NO3)2、AgNO3的混合溶液中,锌先与硝酸银反应生成硝酸锌和银,所以滤液中一定含有硝酸锌解离出的Zn2+,滤液仍为蓝色,说明Cu(NO3)2 溶液剩余,则滤液中一定含有硝酸铜解离出的Cu2+,滤液仍为蓝色,表明可能硝酸铜没有与锌反应,可能全部的锌只与部分硝酸银反应,所以滤液中可能有硝酸银剩余,即滤液中可能含有硝酸银解离出的Ag+,选项正确,故选BD。


 品学双优卷系列答案
品学双优卷系列答案 小学期末冲刺100分系列答案
小学期末冲刺100分系列答案 期末复习检测系列答案
期末复习检测系列答案 超能学典单元期中期末专题冲刺100分系列答案
超能学典单元期中期末专题冲刺100分系列答案科目:初中化学 来源: 题型:
【题目】 如图为金刚、石墨和C60的结构模型图,图中小球代表碳原子。下列说法不正确的是( )
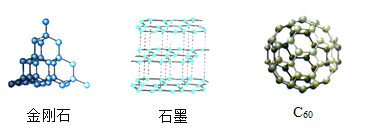
A. 原子的排列方式改变,则构成的物质种类改变
B. 相同元素组成的不同物质,在足量的氧气中完全燃烧,产物相同
C. 相同元素组成的不同物质,化学性质相同
D. 在特定的条件下,石墨既可转化为金刚石,也可转化为C60
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】逻辑推理是化学学习中常用的一种思维方法,以下四个推理中正确的是( )
A.酸碱中和反应生成盐和水,则生成盐和水的反应一定是中和反应
B.化合物都是由不同元素组成的,则不同元素组成的物质一定是化合物
C.含碳元素的物质充分燃烧会生成![]() ,燃烧能生成
,燃烧能生成![]() 的物质一定含碳元素
的物质一定含碳元素
D.离子是带电的粒子,则带电的粒子一定是离子
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某工业废液中含有KCl和CaCl2,如果将该废液中的KCl和CaCl2分离回收变废为宝,设计工艺流程如下图所示,回答问题。

(1)操作2的名称是_____。
(2)写出固体B的化学式_____。
(3)向固体A中加适量稀盐酸的作用是_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】工业上用闪锌矿(主要含ZnS,还含PbS等杂质)制备锌的流程如下图( 部分产物已略去):
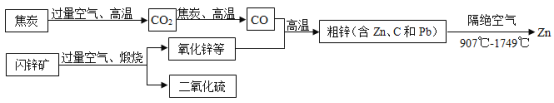
已知: Zn 的沸点为907°C,C的沸点为4827°C,Pb 的沸点为1749°C
(1)制备锌的过程中使用焦炭的作用是生成CO和_____________。
(2) Zn 能与PbCl2溶液反应生成Pb,说明Zn的金属活动性比Pb_____________(填 “弱”或“强”)。
(3)由粗锌制Zn需在“隔绝空气”条件下的原因是______________。
(4)工厂烟气脱硫工艺不仅能消除二氧化硫,还能将其转化为硫酸钙等产品,实现“变废为宝”,原理为![]() 。则吸收上述制备流程中产生的6.4t SO2至少需要含CaCO3 80 %的石灰石多少(写出计算过程)______________ ?
。则吸收上述制备流程中产生的6.4t SO2至少需要含CaCO3 80 %的石灰石多少(写出计算过程)______________ ?
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】燃气热水器是以燃气为燃料,通过燃烧的方式加热制备热水的一种燃气用具。某品牌的一款燃气热水器如下图所示,请回答下列问题:

(1)图中所示材料中,含有的金属元素为_______________(填化学式,写出一种即可),属于有机合成材料的是______________。
(2)燃气热水器常以天燃气为燃料,请写出天然气的主要成分完全燃烧的化学方程式__________。
(3)室内使用燃气热水器易使人中毒,原因是燃气燃烧时易产生________(填化学式)气体。
(4)常见的家用热水器有电热水器、燃气热水器和太阳能热水器,从节约能源和环保的角度看、提倡使用____________热水器。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】银器发暗是因为形成了黑色的Ag2S。欲使银器变亮,可先用洗衣粉洗去表面油污,再把它和铝片放入碳酸钠溶液中共煮,至银器恢复银白色时,取出银器,用水洗净即可。发生反应的化学方程式为:2Al+3Ag2S+6H2O![]() 6Ag+2Al(OH)3+3X↑,X的化学式是
6Ag+2Al(OH)3+3X↑,X的化学式是
A. H2SB. SO2C. SO3D. O2
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】烧碱是一种重要的化工原料,广泛应用于制取肥皂,以及石油、造纸、纺织和印染等工业。
(1)新冠肺炎疫情期间常用的84消毒液的制备离不开烧碱,84消毒液的主要成分是次氯酸钠(NaClO)。烧碱能制备次氯酸钠是因为烧碱能与氯气反应:2NaOH+Cl2=NaClO+X+H2O,其中X的化学式为_____。用途广泛的烧碱还有很多性质,如图表示烧碱与相关物质的关系(箭头表示物质间能转化,实线表示物质间能反应),请回答:
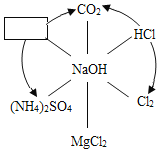
①![]() 中物质的化学式为
中物质的化学式为
②图中物质间发生中和反应的化学方程式为:_____(写出一个即可)。
(2)如图为某化工厂利用苛化法生产烧碱的流程图。“碱泥”曾经是该化工厂最头疼的一种废物,占地堆放对环境造成不利影响。工厂技术人员经过技术革新,变废为宝,使“碱泥”变成了副产品,既解决了占地与环境污染问题,又增加了工厂收入。请分析流程图并回答:
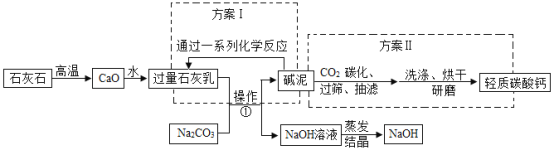
①操作的名称是_____。
②方案Ⅰ的系列反应不涉及的基本反应类型是_____(填序号)。
A化合反应B分解反应C置换反应D复分解反应
③“碱泥”与CO2反应生成碳酸钙的化学方程式为:_____。
④写出图中反应①的化学方程式_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】教育部从2018年开始,要求在学校普及垃圾分类回收处理的相关知识。某化学活动小组结合所学的知识对此进行一系列实践活动。
I.活动探究:
(1)学会识图分拣垃圾:下列垃圾应投入带有如图图标的垃圾箱内的是______ (填字母序号)。

A 塑料瓶
B 果皮
C 碎瓷片
(2)学会检验有害气体:含氯塑料焚烧时会产生氯化氢等气体。若要检验焚烧后的气体中有氯化氢,可将其通入_____________溶液中,有白色沉淀生成即可。
(3)在农村,人们把秸秆、杂草、人畜粪便等废弃物放在密闭的池中发酵可获得沼气,用作燃料,其中沼气的主要成分是_____________(填写化学式)。
II.实验探究:
[提出问题]如何回收处理废旧电池中的镉?
[查阅资料]
(1)废旧电池中含有镉、汞等元素,这些元素会危害人类健康。
(2)镉(Cd)从溶液中析出时呈海绵状固体。在化合物中通常表现为+2价。
(3)碳酸镉(CdCO3)、氢氧化镉Cd(OH)2都是白色固体、难溶于水。
[设计实验]先将废旧电池进行处理以制得硫酸镉(CdSO4)溶液,用于以下实验。
实验设计 | 实验步骤 | 实验现象 | 实验结论 |
与金属反应 | 取少许溶液于试管中,加入足量的Zn粉,充分反应 | _______ | Zn可以置换出Cd |
与碱反应 | 取少许溶液于试管中,加入足量的氢氧化钠溶液,充分及应 | 产生白色沉淀 | 用化学方程式表示为_______ |
与盐反应 | 取少许溶液于试管中,加入足量的__________溶,充分反应。 | 产生白色沉淀 | 可用该试剂除去CdSO4 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com