
| 残留固体的成分 | 探究的步骤 | 可能观察到的现象 | 结论及化学反应方程式 |
| (1)可能有氧化钙. | 取残留固体加水溶解,过滤,向滤液中滴加几滴无色酚酞试液. | 现象: | 结论: |
| (2)还可能有碳酸钙. | 另取残留固体滴加足量盐酸. | ① | 结论: 方程式: |
| ② | 结论: |
分析 根据题设条件,按步分析,逻辑推理,层层推进,“对号入座”,得出结论.
由氧化钙的化学性质、碱与指示剂的反应和碳酸盐与酸的反应可以得出本题的答案.
解答 解:(1)若残留固体中含有氧化钙,氧化钙溶于水时会与水反应生成氢氧化钙,向氢氧化钙溶液中滴入无色酚酞试液,溶液会由无色变成红色.由于滴入无色酚酞试液后溶液确实由无色变成了红色,因此可以确定残留固体中含有氧化钙.
(2)若残留固体中含有碳酸钙,碳酸钙与稀盐酸反应时会有气泡产生.若实验中看到有气泡产生,说明残留固体中含有碳酸钙,反应的化学方程式为:CaCO3+2HCl=CaCl2+H2O+CO2↑;若实验中没有看到气泡产生,说明残留固体中不含碳酸钙.
故答案为:
| 残留固体的成分 | 探究步骤 | 可能观察到的现象 | 结论及化学反应方程式 |
| (1) | 酚酞变红或溶液变红 | 有氧化钙生成 | |
| (2) | ①有气泡产生 | 残留固体中有碳酸钙 CaCO3+2HCl═CaCl2+CO2↑+H2O | |
| ②无气泡产生 | 残留固体中无碳酸钙 |
点评 本题主要考查氧化钙的化学性质、碱与指示剂的反应和碳酸钙与稀盐酸的反应,难度较小.


 智能训练练测考系列答案
智能训练练测考系列答案科目:初中化学 来源: 题型:选择题
| A. | 碳在氧气中燃烧放出白烟 | |
| B. | 硫在氧气中燃烧产生淡蓝色的火焰 | |
| C. | 铁丝在氧气中燃烧生成黑色的四氧化三铁 | |
| D. | 一氧化碳在空气中燃烧产生蓝色火焰 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题

查看答案和解析>>
科目:初中化学 来源: 题型:推断题
 A到G都是初中化学常见的物质,其中C、D、E、F、G属于不同类别的物质,A、C的组成元素相同,C、F中不含有相同的元素,B为红色粉末.它们之间的相互关系如图所示:(其中“--”表示相连物质间能反应,“→”表示两种物之间的转化关系,部分反应物、生成物及反应条件省略).
A到G都是初中化学常见的物质,其中C、D、E、F、G属于不同类别的物质,A、C的组成元素相同,C、F中不含有相同的元素,B为红色粉末.它们之间的相互关系如图所示:(其中“--”表示相连物质间能反应,“→”表示两种物之间的转化关系,部分反应物、生成物及反应条件省略).查看答案和解析>>
科目:初中化学 来源: 题型:选择题
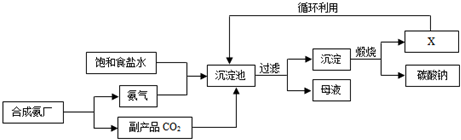
| A. | 沉淀池中的反应物只有两种 | |
| B. | 物质X是氨气,它可以循环使用 | |
| C. | 沉淀为碳酸钙 | |
| D. | 通入氨气的作用是使溶液呈碱性,促进二氧化碳的吸收,更多地析出沉淀 |
查看答案和解析>>
科目:初中化学 来源: 题型:推断题
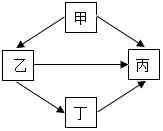 甲、乙、丙、丁为初中化学常见物质,他们之间有如图所示的反应关系(“→”表示一种物质能转化成另一种物质,部分反应物和生成物及反应条件已略去).回答下列问题:
甲、乙、丙、丁为初中化学常见物质,他们之间有如图所示的反应关系(“→”表示一种物质能转化成另一种物质,部分反应物和生成物及反应条件已略去).回答下列问题:查看答案和解析>>
科目:初中化学 来源: 题型:推断题
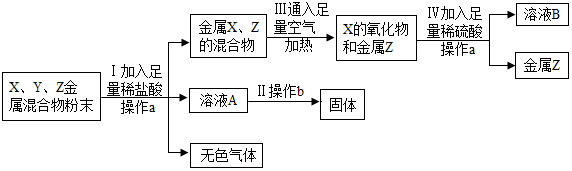
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
| 实验步骤 | 实验现象 | 实验结论 |
| 实验一:取少量溶液于试管中,滴加氯化钙溶液(或稀盐酸) | 产生白色沉淀(或有气泡冒出) | 该溶液是碳酸钠溶液. 有关反应的化学方程式为:CaCl2+Na2CO3═CaCO3↓+2NaCl,(Na2CO3+2HCl═2NaCl+H2O+CO2↑) |
| 实验二:取少量溶液于试管中,滴加硫酸铜溶液 | 产生蓝色沉淀 | 该溶液是氢氧化钠溶液. |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com