
除去下列物质中的少量杂质所选用的试剂或方法正确的是( )
| 选项 | 物质 | 所含杂质 | 所选用试剂或方法 |
| A | NaOH溶液 | Na2CO3 溶液 | 稀盐酸 |
| B | CaO | Ca | 高温灼烧 |
| C | Fe | Zn | 稀硫酸 |
| D | 稀盐酸 | 稀硫酸 | 加适量Ba(NO3)2溶液,再过滤 |
 名校课堂系列答案
名校课堂系列答案科目:初中化学 来源: 题型:
下列有关环境保护的说法中错误的是( )
A.开发新能源,减少使用化石燃料,控制温室效应
B.重复使用塑料制品,减少白色污染
C.提倡金属废弃物回收利用,既能节约金属资源,也可防止污染
D.水 体有自净能力,所以生活污水直接排放也没关系
体有自净能力,所以生活污水直接排放也没关系
查看答案和解析>>
科目:初中化学 来源: 题型:
下列说法正确的是( )
A.金刚石和石墨物理性质差异很大的原因是构成物质的原子结构不同
B.人们常常在铁的表面刷一层铝粉防锈,原因是铝的化学性质不活泼
C.盐酸可用于除铁锈,原因是盐酸可与 金属氧化物反应
金属氧化物反应
D.把Ca(OH)2和NH4Cl一起使用既可改良土壤酸性又可以补充氮肥
查看答案和解析>>
科目:初中化学 来源: 题型:
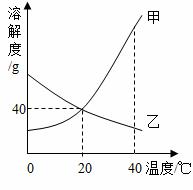
甲和乙两种物质的溶解度曲线如右图。
(1)20℃时,甲物质的溶解度为 ;
(2)20℃时,将甲、乙两物质的饱和溶液各100g,分别升温到40℃,(不考虑水分的蒸发)所得甲物质溶液的质量 (选填“>”或“=”或“<”)乙物质溶液的质量。过滤后再将两溶液恢复至20℃,此时甲物质溶液中溶质的质量分数 (选填“>”或“=”或“<”)乙物质溶液中溶质的质量分数。
(选填“>”或“=”或“<”)乙物质溶液中溶质的质量分数。
(3)A、B两烧杯中分别装有40℃的100g和200g的相同浓度的甲的不饱和溶液,将两份溶液分别都恒温蒸发20g水,都析出了晶体。析出晶体的质量关系为A__________B(选填“>”或“=”或“<”)
查看答案和解析>>
科目:初中化学 来源: 题型:
点燃的火柴竖直向上,火柴梗不易继续燃烧, 其原因是( )
其原因是( )
A. 火柴梗温度达不到着火点 B. 火柴梗着火点较高
C. 火柴梗潮湿不易继续燃烧 D. 火柴梗接触氧气少
查看答案和解析>>
科目:初中化学 来源: 题型:
如图,在试管和小气球中分别先加入稀盐酸和一种常见的固体物质,然后将气球中的固体倒入试管中,观察到有气泡产生且气球胀大。请依据上述实验回答下列问题:

(1)气球中加入的固体物质可能是(至少答出两种不同类型的物质) 、 。
(2)请用简单的实验方法,证明制得的气体的密度比空气大还是小。


查看答案和解析>>
科目:初中化学 来源: 题型:
小明把过量锌粒加入有盐酸的试管中,发现随着反应的进行,产生气体的速度逐渐加快,一段时间后逐渐减慢,最后停止产生气体。在反应过程中,溶液的温度也先随之升高,最后下降到室温。于是,小明设计实验来探究“一定质量的某种金属和同体积盐酸反应快慢的影响因素”。测得实验数据如下:
某金属与同体积盐酸溶液反应实验数据表
| 盐酸溶液浓度 | 反应开始时酸 溶液的温度 | 反应开始到2分钟产生的气体体积 | 反应结束共产生气体体积 |
| 5% | 20℃ | 10 mL | 60 mL |
| 10% | 20℃ | 19 mL | 118 mL |
| 15% | 20℃ | 28 mL | 175 mL |
| 5% | 35℃ | 28 mL | 60 mL |
| 10% | 35℃ | 72 mL | 118 mL |
| 15% | 35℃ | 103 mL | 175 mL |
(1)分析实验数据得出:一定质量的某种金属和同体积盐酸反应,影响金属和酸反应快慢的主要因素有 、 。
(2)可以通过比较 实验数据来确定金属和酸反应的快慢。
(3)过量锌粒加入盐酸中,反应开始的一段时间,反应速率逐渐加快,而不是逐渐减慢。请分析原因。 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com