
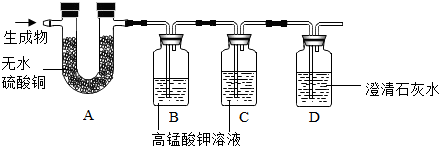
分析 根据题目提供的信息:二氧化硫能使紫色的高锰酸钾溶液褪色,还能使澄清的石灰水变浑浊.以及水能够使无水硫酸铜变成蓝色,二氧化碳可使澄清石灰水变浑浊.分析解答.
解答 解:因为二氧化硫能使紫色的高锰酸钾溶液褪色,还能使澄清的石灰水变浑浊,以及水能够使无水硫酸铜变成蓝色,二氧化碳可使澄清石灰水变浑浊.通入生成物后,观察到A装置中白色粉末变为蓝色;B装置中紫色溶液褪色,说明有水和二氧化硫生成;如果观察到C中的高锰酸钾不褪色(生成物中的二氧化硫与B中高锰酸钾溶液反应,不会再与C中的高锰酸钾反应),而D中的澄清石灰水变浑浊,说明有二氧化碳生成.
故答案为:B装置中紫色溶液褪色;高锰酸钾溶液不褪色.
点评 本题解题的关键是了解常见物质二氧化碳、水的特性,以及题目提供的信息.


科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| 类别 | 物质 |
| 甲 | 氯化钠、水 |
| 乙 | 氧气、铜 |
| A. | 甲为化合物,乙为单质 | B. | 甲为单质,乙为化合物 | ||
| C. | 甲为氧化物,乙为金属 | D. | 甲为金属,乙为氯化物 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
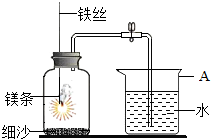 某校研究性学习小组探究空气中氧气的体积分数,他们想选用以下药品进行实验:①木炭;②红磷;③铁丝;④镁条.
某校研究性学习小组探究空气中氧气的体积分数,他们想选用以下药品进行实验:①木炭;②红磷;③铁丝;④镁条.查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 乙酸乙酯是一种混合物 | |
| B. | 乙酸乙酯是由碳、氢、氧三种元素组成的 | |
| C. | 乙醇中碳、氢、氧三种元素的质量比为2:4:1 | |
| D. | 乙酸乙酯中只有氧元素显负价 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com