

分析 【提出问题】氢氧化钠吸收了空气中二氧化碳而生成新的物质碳酸钠;
【实验探究】根据所学知识可以知道,若氢氧化钠变质则会生成碳酸钠,碳酸钠溶液显碱性,也就是说我们可以根据判断是不是含有碳酸钠来检验氢氧化钠是否变质,所以本题名义上是验证氢氧化钠是否变质,实际上就是碳酸盐的检验,故可以根据这方面的知识来解答该题;
(1)由于碳酸钠溶液呈碱性,影响使用酚酞对氢氧化钠的检验,因此首先使用足量氯化钙等物质,充分反应沉淀掉溶液中的碳酸钠且不形成碱性物质,然后滴加酚酞检验溶液中的氢氧化钠;
(2)过滤适用于不溶于水的固体和液体分离;
(3)用pH试纸测定未知溶液的pH时,正确的操作方法为用玻璃棒蘸取少量待测液滴在干燥的pH试纸上,与标准比色卡对比来确定pH.不能用水湿润pH试纸,否则稀释了待测溶液,使溶液的酸碱性减弱,测定结果不准确;
【交流反思】(1)结合浓硫酸的性质进行填空;
(2)在检验并除去碳酸钠时,不应使用呈碱性的溶液或反应后能生成碱性物质的试剂,避免对后面滴入酚酞进行氢氧化钠的检验.
解答 解:【提出问题】氢氧化钠与空气中的二氧化碳反应生成碳酸钠和水,而使氢氧化钠变质,故反应的化学方程式为:2NaOH+CO2═Na2CO3+H2O;
【实验探究】根据所学知识可以知道,若氢氧化钠变质则会生成碳酸钠,碳酸钠溶液显碱性,也能使酚酞溶液变红,因此小刚同学的实验方案错误;
(1)实验操作④是将沉淀与液体分开,此操作是过滤,玻璃棒的作用是引流;
(2)步骤③中,防止碳酸钠对氢氧化钠检验的影响,可采取加入过量氯化钙溶液的方法把碳酸钠全部转变成沉淀,以检验溶液中是否还含有氢氧化钠,若有氢氧化钠则判断为部分变质;
(3)步骤⑤中,用pH试纸测定未知溶液的pH时,正确的操作方法为用玻璃棒蘸取少量待测液滴在干燥的pH试纸上,与标准比色卡对比来确定pH.小敏用洁净干燥的玻璃棒蘸取某溶液滴到湿润的pH试纸上,测得pH=10.由于用水湿润pH试纸,稀释了该碱性溶液,溶液的碱性变弱,故小明同学的测定结果偏小.
【交流反思】(1)浓硫酸需要密封保存的原因是有吸水性;
(2)为不影响滴加酚酞对氢氧化钠是否存在的检验,所加入的试剂不应为碱性溶液且不能反应后生成碱性物质,而氢氧化钙、氢氧化钡都呈碱性且能与碳酸钠反应生成氢氧化钠,因此,不能使用③Ca(OH)2溶液、④Ba(OH)2溶液代替氯化钙溶液;
故答案是:【提出问题】CO2+2NaOH=Na2CO3+H2O
【实验探究】若变质,则生成的Na2CO3其溶液也呈碱性
(1)过滤 引流
(2)使Na2CO3完全反应,排除干扰(或证明并完全除去Na2CO3)
(3)D
【交流反思】(1)浓硫酸有很强的吸水性
(2)①②(答全给分)
点评 本题中要知道氢氧化钠变质的原因,要熟练掌握实验室中检验碳酸盐的方法,检验氢氧化钠与碳酸钠的混合物时,可先把碳酸钠变成沉淀并且不生成影响氢氧化钠检验的碱性物质,然后使用酚酞检验氢氧化钠.


科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | A2B4 | B. | AB3 | C. | A3B2 | D. | A2B |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 盐酸溶 液浓度 | 反应开始时 酸溶液的温度 | 反应开始到2分钟 产生的气体体积 | 反应结束共产生气体体积 |
| 5% | 20°C | 10ml | 60ml |
| 10% | 20°C | 19ml | 118ml |
| 15% | 20°C | 28ml | 175ml |
| 5% | 35°C | 28ml | 60ml |
| 10% | 35°C | 72ml | 118ml |
| 15% | 35°C | 103ml | 175ml |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 实验编号 | 1 | 2 |
| 反应物 | 6% 过氧化氢溶液 | 6% 过氧化氢溶液 |
| 催化剂 | 1g红砖粉 | 1g 二氧化锰 |
| 时间 | 152s | 35s |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
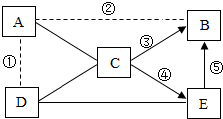 A~E是碳单质、氧化铜、氧气、二氧化碳、一氧化碳五种物质中的某一种A、C是黑色固体,B、D、E是无色气体,它们之间的相互关系如图所示(实连线“-”表示物质间能反应,虚连线“---”表示物质间不能反应,箭头“→”表示物质间的转化关系).请回答下列问题:
A~E是碳单质、氧化铜、氧气、二氧化碳、一氧化碳五种物质中的某一种A、C是黑色固体,B、D、E是无色气体,它们之间的相互关系如图所示(实连线“-”表示物质间能反应,虚连线“---”表示物质间不能反应,箭头“→”表示物质间的转化关系).请回答下列问题:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com