
分析 根据题干提供的信息结合物质的性质进行分析解答,
①取少量样品溶于水得到无色溶液,滴加稀盐酸有气泡产生;说明一定含有碳酸钾,一定不含有硫酸铜和氯化钙;
②取少量样品于试管中滴加过量的氯化钡溶液,出现白色沉淀A,过滤.沉淀A中加入过量的稀硝酸,沉淀部分消失并放出气体,说明一定含有硫酸钾;
③往步骤②所得的滤液中加入适量硝酸银溶液和稀硝酸,生成白色沉淀B,过滤,不一定含有氯化钾,据此解答.
解答 解:①取少量样品溶于水得到无色溶液,滴加稀盐酸有气泡产生;说明一定含有碳酸钾,一定不含有硫酸铜和氯化钙;
②取少量样品于试管中滴加过量的氯化钡溶液,出现白色沉淀A,过滤.沉淀A中加入过量的稀硝酸,沉淀部分消失并放出气体,说明一定含有硫酸钾;
③往步骤②所得的滤液中加入适量硝酸银溶液和稀硝酸,生成白色沉淀B,过滤,由于计入氯化钡的时候引入了氯离子,故不一定含有氯化钾;
(1)硝酸银能与含有氯离子的物质结合产生氯化银沉淀,故填:氯化银;
(2)一定含有碳酸钾和硫酸钾,一定不含有硫酸铜和氯化钙,故填:碳酸钾和硫酸钾;硫酸铜和氯化钙;
(3)氯化钡能与碳酸钾反应生成碳酸钡沉淀,碳酸钡能与硝酸反应生成硝酸钡、水和二氧化碳,故填:BaCO3+2HNO3═Ba(NO3)2+H2O+CO2↑.
点评 在解此类题时,首先分析题中所给物质的性质和两两之间的反应,然后依据题中的现象判断各物质的存在性,最后进行验证即可.


 应用题作业本系列答案
应用题作业本系列答案科目:初中化学 来源: 题型:选择题
| A. | 生铁不是纯铁,而钢是纯铁 | |
| B. | 铝制品抗腐蚀能力较铁制品强 | |
| C. | 铁在氧气中燃烧生成氧化铁 | |
| D. | 用FeSO4溶液、Cu和Ag三种物质可以验证Fe、Cu、Ag三种金属的活动性强弱顺序 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题

| A.过氧化氢溶液和二氧化锰混合 | B.加热高锰酸钾 |
 |  |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
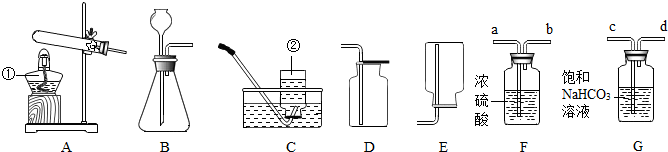
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
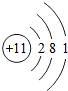 如图为某元素一种粒子的结构示意图,下列说法错误的是( )
如图为某元素一种粒子的结构示意图,下列说法错误的是( )| A. | 该粒子是原子的结构示意图 | B. | 该粒子的核电荷数为1 | ||
| C. | 该元素属于金属元素 | D. | 该粒子在化学反应中容易失去电子 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题

查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
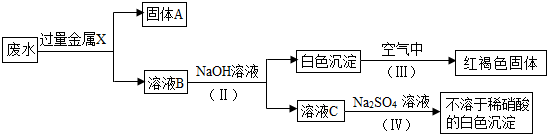
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
 向硫酸铜和盐酸的混合溶液中,逐滴加入NaOH溶液,产生沉淀的质量与所滴入NaOH溶液的质量关系如图所示.则C点时,溶液中的溶质是(填化学式)NaCl;Na2SO4;NaOH.
向硫酸铜和盐酸的混合溶液中,逐滴加入NaOH溶液,产生沉淀的质量与所滴入NaOH溶液的质量关系如图所示.则C点时,溶液中的溶质是(填化学式)NaCl;Na2SO4;NaOH.查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
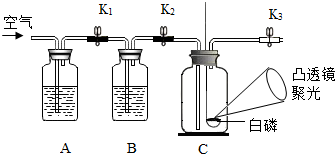 学习了工业上分离液态空气制取氧气的方法之后,某学习小组在探究“从空气中制取氮气”时,提出了以下实验方案,并设计了如下实验装置图:(假设每步反应都能把气体充分除去)
学习了工业上分离液态空气制取氧气的方法之后,某学习小组在探究“从空气中制取氮气”时,提出了以下实验方案,并设计了如下实验装置图:(假设每步反应都能把气体充分除去)查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com