解:已知B是黑色固体、相对分子质量为80,从所学的黑色固体主要有碳、氧化铜、二氧化锰等,而这些物质中相对分子质量为80的只有氧化铜,E是天然气的主要成份,所以E是甲烷,A通电能够分解,则A是水,B能够由C制得且C是水的分解产物,所以C是氧气,D是甲烷反应的产物,所以D是二氧化碳(可由甲烷的燃烧制得也可由碳和氧气反应制得);
(1)由分析知B是CuO,E是CH
4;
(2)A→C是水的电解过程,该反应的化学方程式为2H
2O

2H
2↑+O
2↑;E→D是甲烷燃烧的过程,化学方程式为CH
4 +2O
2
CO
2 +2H
2O,B→A属复分解反应时生成水,则该反应是氧化铜和稀酸的反应,化学方程式可以是CuO+H
2SO
4=CuSO
4+H
2O;
(3)若B→A属置换反应,则该反应可能是氢气和氧化铜的反应,产物的固体是红色的铜,由于在发生置换过程可能发生副反应产生Cu
2O,产物为红色固体,所以产物的固体可能是铜或氧化亚铜或两者的混合物,故其产物组合可能有三种,由于氧化铜和硫酸反应后固体能够完全溶解,所以小思同学称取14.4g产物与足量稀硫酸充分反应后,经过滤、干燥.得到8.6g固体能说明该固体中一定含有氧化亚铜,假设14.4g固体全部是氧化亚铜,则设该反应生成铜的质量是x
Cu
2O+H
2SO
4═Cu+CuSO
4+H
2O
144 64
14.4g x
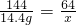
x=6.4g
由生成的固体质量是8.6g可知该产物中一定含有铜和氧化亚铜两种;
故答案为:(1)CuO;CH
4;(2)2H
2O

2H
2↑+O
2↑;CH
4 +2O
2
CO
2 +2H
2O;CuO+H
2SO
4=CuSO
4+H
2O;(3)三;CuO、Cu
2O;
分析:已知B是黑色固体、相对分子质量为80,从所学的黑色固体主要有碳、氧化铜、二氧化锰等,而这些物质中相对分子质量为80的只有氧化铜,E是天然气的主要成份,所以E是甲烷,A通电能够分解,则A是水,B能够由C制得且C是水的分解产物,所以C是氧气,以此为突破口分析解答即可.
点评:此题为框图式物质推断题,完成此类题目,关键是找准解题突破口,直接得出结论,然后利用顺向或逆向或两边向中间推,逐一导出其他结论.

 如图,A、B、C、D、E是初中化学中常见的物质,转化关系(其中部分生成物和反应条件已忽略):已知B是黑色固体、相对分子质量为80,E是天然气的主要成份.请回答下列问题:(1)B是______E是______(均填化学式).
如图,A、B、C、D、E是初中化学中常见的物质,转化关系(其中部分生成物和反应条件已忽略):已知B是黑色固体、相对分子质量为80,E是天然气的主要成份.请回答下列问题:(1)B是______E是______(均填化学式). 2H2↑+O2↑;E→D是甲烷燃烧的过程,化学方程式为CH4 +2O2
2H2↑+O2↑;E→D是甲烷燃烧的过程,化学方程式为CH4 +2O2 CO2 +2H2O,B→A属复分解反应时生成水,则该反应是氧化铜和稀酸的反应,化学方程式可以是CuO+H2SO4=CuSO4+H2O;
CO2 +2H2O,B→A属复分解反应时生成水,则该反应是氧化铜和稀酸的反应,化学方程式可以是CuO+H2SO4=CuSO4+H2O;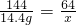
 2H2↑+O2↑;CH4 +2O2
2H2↑+O2↑;CH4 +2O2 CO2 +2H2O;CuO+H2SO4=CuSO4+H2O;(3)三;CuO、Cu2O;
CO2 +2H2O;CuO+H2SO4=CuSO4+H2O;(3)三;CuO、Cu2O;

 计算高手系列答案
计算高手系列答案 (2009?聊城)如图是a、b、c、d四种固体物质的溶解度曲线;下表是这些固体物质在部分温度时的溶解度.
(2009?聊城)如图是a、b、c、d四种固体物质的溶解度曲线;下表是这些固体物质在部分温度时的溶解度. 20、如图是a、b、c、d四种固体物质的溶解度曲线;图表是这些固体物质在部分温度时的溶解度.根据图表信息判断下列说法正确的是( )
20、如图是a、b、c、d四种固体物质的溶解度曲线;图表是这些固体物质在部分温度时的溶解度.根据图表信息判断下列说法正确的是( ) 2012年奥运会将在英国伦敦举行.奥运五环代表五大洲人们手拉手和睦相处.如图,A、B、C、D、E各代表铁、水、二氧化碳、硫酸铜溶液、氢氧化钙溶液中的一种物质.常温下,相连环物质间能发生反应,不相连环物质间不能发生反应,且B的相对分子质量大于D.请填空:
2012年奥运会将在英国伦敦举行.奥运五环代表五大洲人们手拉手和睦相处.如图,A、B、C、D、E各代表铁、水、二氧化碳、硫酸铜溶液、氢氧化钙溶液中的一种物质.常温下,相连环物质间能发生反应,不相连环物质间不能发生反应,且B的相对分子质量大于D.请填空: 如图,A、B、C、D、E、F均是初中化学的常见物质,A、B、C均含有同一种元素,B、C、D是气体,A、E是黑色固体,变化①的现象是颜色由黑变红,变化②的现象是颜色由红变黑,相应变化的生成物没有全部列出,各变化的条件也未标出.
如图,A、B、C、D、E、F均是初中化学的常见物质,A、B、C均含有同一种元素,B、C、D是气体,A、E是黑色固体,变化①的现象是颜色由黑变红,变化②的现象是颜色由红变黑,相应变化的生成物没有全部列出,各变化的条件也未标出.