
【题目】烧杯中盛有一定质量的MgO 和MgCO3固体混合物中,向其中加入稀硫酸100g ,恰好完全反应,得到104g 该温度下的不饱和溶液。该不饱和溶液的质量分数最接近的是( )
A. 11.5% B. 18.9% C. 5.1% D. 25.9%
科目:初中化学 来源: 题型:
【题目】人类的生活和生产都离不开金属。
(1)秦朝铸造的青铜剑经分析,其成分有铜、锡及少量的铅、铁等。青铜属于_______。
A.合成材料 B.复合材料 C.金属材料 D.非金属材料
(2)高炉炼铁的反应之一是氧化铁与一氧化碳反应,写出这个反应的化学方程式_______。
(3)公园的铁制扶手栏杆容易锈蚀,防锈方法之一是_______。铝的金属活动性比铁强,但铝不容易锈蚀,原因是_______。
(4)参考钠原子的结构示意图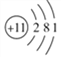 ,画出钠离子(Na+)的结构示意图_______。
,画出钠离子(Na+)的结构示意图_______。
(5)钛酸锂(Li4Ti5O12)是制造锂电池的材料之一,其中锂、钛两种元素的质量比是______,配平制取钛酸锂的化学方程式:___TiO2+ ___Li2CO3 高温___Li4Ti5O12+___CO2↑
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某化学小组将刚制取的二氧化碳气体通入含有少量过氧化钠(Na2O2)粉末(过氧化钠为淡黄色固体)的玻璃管中,看到玻璃管另一端有气泡冒出,同时粉末由淡黄色变为白色。
【提出问题】
过氧化钠与二氧化碳是否反生反应?生成了什么物质?
【作出猜想】
甲同学:没反应,冒出的还是二氧化碳气体
乙同学:发生反应,生成碳酸钠
丙同学:发生反应,生成一氧化碳
丁同学:发生反应,生成氧气
(1)大家一致认为甲同学的推测不正确,理由是________________________。
【实验探究】

__________________ __________________ ________________
【得出结论】
(5)过氧化钠与二氧化碳反应的化学方程式为____________________________________。
【反思拓展】
(6)根据过氧化钠的这一性质,请你设想过氧化钠的一种用途___________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】为测定某稀硫酸的溶质的质量分数,小兰同学设计了如下实验方案.
![]()
第②步实验中生成沉淀的质量与加入NaOH溶液的质量关系如图.
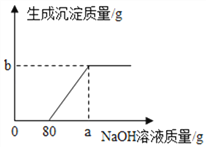
(1)分析第②步实验:与先加入的80g NaOH溶液反应的物质是_____(填化学式),继续加入NaOH溶液后产生的沉淀是_____(填名称)
(2)计算稀硫酸的溶质的质量分数______________(写出计算过程)
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】我国拥有丰富的海洋资源,我们可以从海水中提取食盐,并以此为原料制得具有广泛用途的产品。
(1)海水晒盐是利用了_____的方法使食盐晶体析出,得到粗盐。
(2)某制碱工厂以粗盐为原料制纯碱,部分工艺流程如下: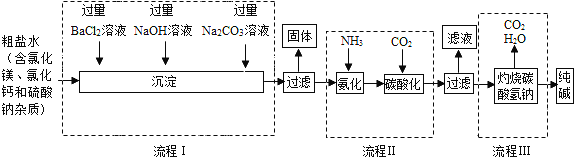
①流程I中为了除去杂质,依次加入过量BaCl2溶液、NaOH溶液和Na2CO3溶液,下列说法正确的是_____(填字母编号);
A.加入三种溶液的顺序不能调整
B.加入三种溶液可将粗盐水中的SO4、Mg2+、Ca2+转化为沉淀
C.按流程I所加溶液的顺序除杂,过滤后得到四种沉淀
②在流程I中,加入氢氧化钠溶液时发生反应的化学方程式是_____;
③流程I中Na2CO3溶液的作用是_____;
④写出流程Ⅲ中发生反应的化学方程式_____。
(3)将已配制好的100g质量分数为6%的氧化钠溶液变成质量分数为20%的氯化钠溶液,需要再加入NaCl的质量是_____g。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】工业铁红主要成分是Fe2O3,还含有少量的FeO、Fe3O4
【查阅资料】(1)草酸晶体(H2C2O43H2O)在浓硫酸作用下受热分解,化学方程式为:H2C2O43H2O ![]() CO2↑+CO↑+H2O
CO2↑+CO↑+H2O
(2)碱石灰是固体NaOH和CaO的混合物,能吸收水蒸气和二氧化碳。
(3)铁的常见氧化物中铁的质量分数:
铁的氧化物 | FeO | Fe2O3 | Fe3O4 |
铁的质量分数 | 77.8% | 70.0% | 72.4% |
【问题讨论】为了测定铁红中铁的质量分数,小组间进行如下实验。(装置气密性良好)
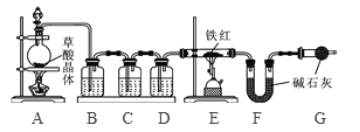
(1)该实验为了保证进入E中的气体是纯净、干燥的CO,则B、C、D中的试剂依次是________(填字母序号)
a.浓硫酸 b.澄清的石灰水 c氢氧化钠溶液
(2)C装置的作用是 __________________________。
(3)写出E装置中所发生反应的一个化学方程式: _____________________。
(4)称取铁红样品10.0g,用上述装置进行实验,测定铁红中铁的质量分数。
①若E中充分反应后得到铁粉的质量为mg,则 ____ < m < ______。
②若实验前后称得F装置増重7.7g,则此铁红中铁的质量分数是 _________。
【实验反思】 (1)如果缺少G装置(不考虑其他因素),则测得样品中铁的质量分数会 ________(选填“偏小”“不变”“偏大”)。
(2)该实验装置的一个明显缺陷是 ___________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】阅读下面短文,回答相关问题。
生活中你是否遇到过这样的事情:你将苹果去皮、切块儿,等待妈妈下班回来。可是一段时间后,苹果块儿表面会生成一种褐色的物质,口感也不那么脆了......变化其实来自于苹果中存在的一种原本无色的多酚类的物质。这类物质能跟氧气结合,产生一些有色物质,这就是褐变过程。
防止苹果发生褐变过程的方法有很多。
碳酸氢钠是一种安全、价格低廉的化学物质,能够直接抑制水果病原真菌的生长,常用于水果贮藏保鲜。选择新鲜、大小均匀、无虫害无伤的苹果果实,消毒、清洗后切成12片,每片厚度约为15mm。切片立即浸泡于下表中的碳酸氢钠溶液中进行保鲜处理。每种浓度的碳酸氢钠溶液中浸泡2块苹果切片。5分钟后将苹果切片捞出、甩干,将12片苹果装在一个塑料保鲜盒中,置于4℃贮藏观察。
1 | 2 | 3 | 4 | 5 | 6 | |
碳酸氢钠溶液的溶度g/L | 0 | 0.5 | 2.0 | 5.0 | 10.0 | 15.0 |
pH | 7.01 | 8.00 | 8.12 | 8.20 | 8.25 | 8.33 |
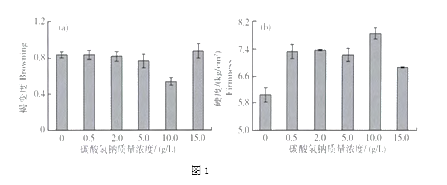
在贮藏3天后,取样测定其褐变度和硬度变化,记录的数据如下图1。
(注:褐变度表示苹果褐变的程度,数值越大褐变程度越高;硬度表示苹果的酥脆程度,数值越大说明越酥脆)
抗坏血酸(即维生素C)是一种抗氧化剂,也可以有效抑制苹果切分后褐变和变软。抗坏血酸在酸性环境下稳定,但是很难发挥抗氧化作用,在弱碱性环境下可以发挥很强的抗氧化作用。而苹果果实的pH一般在3.0~3.8。
取三组苹果切片,分别用10g/L某常用食品防腐剂、10g/L碳酸氢钠与10g/L抗坏血酸的混合液、对照液(蒸馏水)处理,4℃贮存并观察,记录数据如下图2:
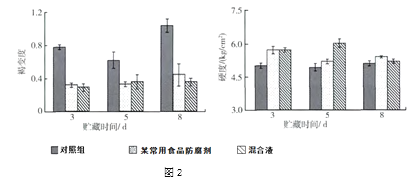
依据文章回答下列问题。
(1)苹果褐变的过程属于____变化(填“物理”或“化学”)。
(2)碳酸氢钠的俗称是_____(填序号)。
A.食盐 B.纯碱 C.小苏打 D.苛性钠
(3)由图1可知,用____ g/L碳酸氢钠溶液处理对鲜切苹果的褐变、变软抑制的效果更好。
(4)由实验可知:抗坏血酸溶液与碳酸氢钠溶液混用效果更好,试推测可能的原因是:_________。
(5)根据文中的实验数据,你对储存苹果切片有哪些建议_________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】A~F六种物质共含H、C、O、N、Ca、Cu六种元素,分别为非金属单质、金属氧化物、非金属氧化物、酸、碱、盐中的一种。其中,A为温室气体,BC均为黑色固体,盐中不含金属。相邻物质之间能发生化学反应。
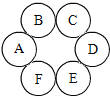
(1)A的固体俗称是_______________;
(2)E与F反应的现象是_________________________________;
(3)C与D反应的化学方程式____________________________________,属于________反应(填基本反应类型)。
(4)除相邻物质之间能发生化学反应外,还能相互反应的化学方程式____________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某小组通过电解水和氢气燃烧两个反应探究水的组成,过程如下。下列分析正确的是( )
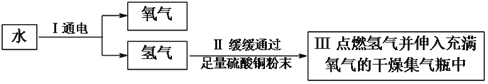
A. 步骤Ⅰ中正、负极产生气体的体积比为2:1
B. 步骤Ⅰ说明水由氢气和氧气组成
C. 步骤Ⅱ的目的是检验并除去氢气中的水蒸气
D. 理论上步骤Ⅰ中参加反应的水和步骤Ⅲ中生成的水质量相等
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com