
【题目】某课外活动小组欲对铝镁合金进行研究,测定其中镁的质量分数。
(查阅资料)
①氢氧化镁和氢氧化铝均难溶于水。难溶性碱受热后能分解生成水和相应的金属氧化物。
②镁和氢氧化镁均不能与氢氧化钠溶液反应,但铝和氢氧化铝分别能与氢氧化钠溶液发生如下反应:2Al+2NaOH+2H2O=2NaAlO2+3H2↑;Al(OH)3+NaOH=NaAlO2+2H2O.氯化铝可与过量氢氧化钠溶液发生反应AlCl3+4NaOH=NaAlO2+3NaCl+2H2O。
(方案设计)
他们利用实验室提供的盐酸、氢氧化钠溶液设计了三种不同的实验方案:
方案一:![]()
方案二:![]()
方案三:![]()
(方案评价)
(1)方案三中最后的灼烧产物的主要成分为水和______(用化学式表示)
(2)小段认为三个方案理论上均可行,但方案三不如其他方案,理由是______。
(实验设计)
实验小组根据方案二设计了如图所示(图中的铁架台已省略)的实验装置。
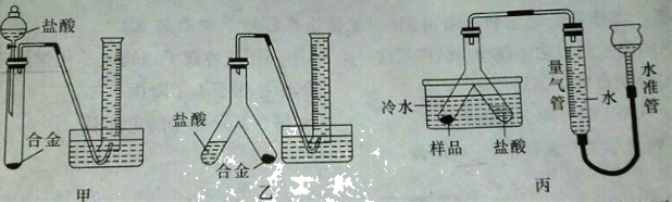
(3)你认为选择装置______(填“甲”或“乙”)测定镁的质量分数更合理,误差更小,理由是______。
(4)若装置丙中不使用冷水,则所测得气体的体积会______(填“偏大”“偏小”或“不变”)。
(交流讨论)
(5)实验小组成员通过交流讨论后重新设计了方案:①称取铝镁合金质量;②加入足量的______;③过滤④洗涤;⑤干燥;⑥称取剩余固体的总质量。
【答案】MgO 操作复杂 乙 甲中滴加的盐酸占据一定的体积 偏大 氢氧化钠溶液
【解析】
(1)方案三中最后的灼烧产物的主要成分为氢氧化镁受热分解生成的水和氧化镁。故填:MgO。
(2)小段认为三个方案理论上均可行,但方案三不如其他方案,通过比较可知,操作三操作比其他方案更为复杂,。故填:操作复杂。
(3)通过比较可知,甲中滴加的盐酸占据一定的体积,导致测定的气体体积偏大,因此选择装置乙测定镁的质量分数更合理,误差更小;故填:乙;甲中滴加的盐酸占据一定的体积。
(4)由于金属和盐酸反应放热,若装置丙中不使用冷水,温度升高会导致气体膨胀,则所测得气体的体积会偏大。故填:偏大。
(5)除了三种方案外,还可以采取的方法是把镁铝合金中的铝用氢氧化钠反应掉,剩余的就是镁了,直接称量镁的质量即可。因此可以重新设计了如下方案:①称取铝镁合金质量;②加入足量的氢氧化钠溶液;③过滤④洗涤;⑤干燥;⑥称取剩余固体的总质量(镁的质量)。故填:氢氧化钠溶液。


科目:初中化学 来源: 题型:
【题目】观察比较与归纳是学习化学的重要方法。对于以下三个化学方程式:2Mg +O2![]() 2MgO;2H2 + O2
2MgO;2H2 + O2![]() 2H2O;2CO + O2
2H2O;2CO + O2![]() 2CO2。
2CO2。
(1)通过比较,发现它们有许多共同点:请你写出其中两点:① _____________ ;② _______________。
(2)以上化学方程式也有许多不同之处,请你写出其中一个与另两个的一点不同之处 ___________ 。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图是实验室制取气体的常用实验装置,根据所学知识回答下列问题。

(1)写出用A装置制取氧气的一个化学方程式______。
(2)利用最优的反应原理制取并收集一瓶干燥的氧气,组装装置可以按顺序选用图中的______(填字母序号)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】人类的日常生活和工农业生产离不开水。请回答:
(1)某地下水中含有较多可溶性钙、镁矿物质,该水属于____(填“软水”或“硬水”)。
(2)自然界中的水一般要净化后才能使用,在沉降、过滤、吸附蒸馏等净水方法中,单一操作相对净化程度最高的是_____。
(3)从海水中提炼出来的重水(化学式为D2O)中重氢原子(D)的相对原子质量是2,则重水中氧元素的质量分数为___________。
(4)下列关于水的说法中,不正确的是_____
A.水是由氢气和氧气组成
B.洗菜、洗衣后的水用来冲洗厕所
C.水通电分解时,水分子的能量没有发生变化
D.合理施用农药、化肥,以减少水体污染
查看答案和解析>>
科目:初中化学 来源: 题型:
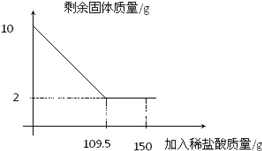
【题目】有一赤铁矿样品(主要成分为Fe2O3),某学校化学兴趣小组为了测得样品中氧化铁的质量分数,进行了如下探究:小明取10g赤铁矿样品(杂质不溶于水和酸),不断加入稀盐酸到固体的质量不再减少,加入稀盐酸的量如图所示:求:
(1)赤铁矿中氧化铁的质量分数是 ;
(2)计算所使用的稀盐酸的溶质质量分数。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】(8分)有一包粉末,已知由CaCO3、FeCl3、MgCl2、Na2SO4、NaOH、NaNO3中的几种组成。为确定其组成,现进行以下实验,各步骤均已充分反应。
①取一定质量的粉末,加水搅拌后过滤,得到沉淀和无色溶液A;
②向①步得到的沉淀中加入足量稀盐酸,得到无色气体和黄色溶液;
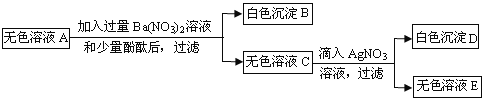
③将①步得到的无色溶液A进行如下图所示的实验。
请回答下列问题:
(1)B的化学式是 。
(2)A中一定存在的溶质的化学式是 。
(3)生成白色沉淀D的化学方程式是 。
(4)这包粉末中可能含有物质的化学式是 。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】在密闭容器中有甲、乙、丙、丁四种物质,在一定条件下反应,测得反应前及反应过程中两个时刻各物质的质量如图所示,图中a、b、c、d分别表示相应物质的质量。下列说法正确的是( )
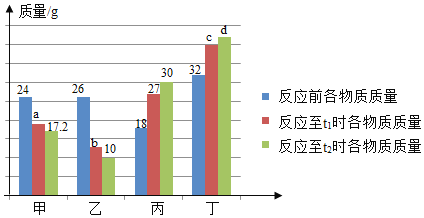
A. b的数值为14
B. 该反应为复分解反应
C. 反应过程中乙与丁发生改变的质量比为5:6
D. 充分反应后生成丙的质量为37.5g
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下表是Ca(OH)2和NaOH的溶解度数据.请回答下列问题:
温度/℃ | 0 | 20 | 40 | 60 | 80 | 100 |
溶解度/g | ||||||
Ca(OH)2 | 0.19 | 0.17 | 0.14 | 0.12 | 0.09 | 0.08 |
NaOH | 31 | 91 | 111 | 129 | 313 | 336 |
(1)依据上表数据,绘制Ca(OH)2和NaOH的溶解度曲线,图中能表示NaOH溶解度曲线的是_____(填“A”或“B”).
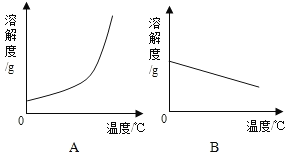
(2)要想把一瓶接近饱和的Ca(OH)2溶液变成饱和溶液,可采取措施有_____(填序号).
①蒸发水 ②升高温度 ③降低温度 ④加入水 ⑤加入氢氧化钙
(3)现有60℃时含Ca(OH)2和NaOH两种溶质的饱和溶液,若要得到较纯净的NaOH晶体,应采取的物理方法是_____.
(4)现有20℃时Ca(OH)2的饱和溶液(甲溶液),向其中加入一定量CaO后恢复20℃,得到乙溶液,溶液中溶质的质量分数的关系为甲_____乙(填“>”“<”或“=”).
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】实验员王老师要配制80克质量分数为10%的NaCl溶液供同学们使用,如图表示了他的实验操作过程。
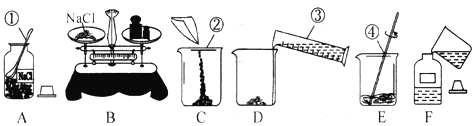
回答下列问题:
(1)写出标号①-④各仪器的名称。①_____②_____③_____④_____
(2)B操作中应称NaCl的质量是_____g,称量时若指针偏右,应进行的操作是_____;
(3)D操作中仪器③的规格应是_____(选填“50ml”或“100ml”),读数时应使视线与_____;
(4)E操作中④的作用是_____;
(5)下列错误操作可能导致溶质的质量分数偏小的是_____(填序号);
①B操作中砝码与NaCl放颠倒了 ②D操作中仰视凹液面最低处读数;
③D操作中有少量水溅出 ④F操作中溶液洒落。
(6)配制该溶液的正确步骤应是_____(填序号)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com