
【题目】下列各组离子在水中一定能大量共存,并形成无色透明溶液的是
A.Na+、Fe3+、NO3-、OH- B.H+、K+、NO3-、HCO3-
C.K+、Ba2+、MnO4-、SO42- D.H+、NH4+、Cl-、SO42-
科目:初中化学 来源: 题型:
【题目】用H、C、O、Cl、Ca五种元素中的一种或几种组成物质,回答下列问题。
(1)写出一种单质的化学式 。
(2)某气体能在氧气中燃烧,生成的物质与该气体组成元素相同,该气体是 _。
(3)氢、氧两种元素组成的甲物质可发生分解反应,其微观示意图如下,请在方框内画出丙的微粒图示。

(4)按下图装置进行实验(气密性良好),将液体滴入瓶中,关闭活塞。请根据表中现象,写出符合要求的物质。

查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】实验室中有一瓶久置的氢氧化钠溶液,以下实验设计合理的是
序号 | 实验目的 | 实验操作 |
① | 证明溶液发生变质 | 取少量溶液,加入足量稀盐酸 |
② | 确定溶液中溶质的成分 | 取少量溶液,加入适量氢氧化钡溶液,过滤,向滤液中滴加酚酞溶液 |
③ | 测定溶液中碳酸钠的质量分数 | 取一定质量溶液,加入足量稀盐酸,将生成的气体通入浓硫酸,测浓硫酸的增重 |
④ | 除去溶液中的碳酸钠 | 向溶液中滴加氢氧化钡溶液至恰好完全反应,过滤 |
A.①② B.②③ C.①④ D. ②④
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】实验小组同学用下面仪器完成如下实验,根据下图回答问题。
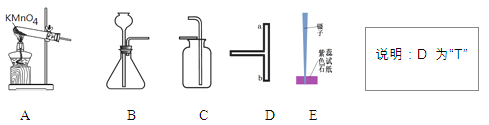
(1)A与C连接,A中发生反应的化学方程式为_____________,用C装置收集气体,将带火星的木条置于集气瓶口,若观察到_________,说明气体已经收集满。
(2)B与D相连,制备二氧化碳并用镊子夹持一块儿紫色石蕊试纸(如图E),证明二氧化碳密度比空气密度大且能与水反应生成酸,其操作步骤为________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】春节期间燃放烟花爆竹会使空气中有害气体SO2的含量增加,为粗略测定空气中SO2的含量,化学小组的同学们设计了如下图所示的实验装置进行实验:

【资料】
①SO2+I2+2H20=H2SO4+2HI,碘遇淀粉能使淀粉显蓝色,而HI溶液不能使淀粉显蓝色。
②我国空气质量标准中SO2浓度限值(mg/m3)如下表;
一级标准 ≤0.15
二级标准 ≤0.50
三级标准 ≤0.70
【实验步骤】
①检查气密性;
②向C装置中加入1.0mL溶质质量分数为1.27×10﹣6 g/mL的碘水(ρ≈1.0g/mL),滴入2~3滴淀粉溶液,此时溶液显蓝色;
③打开弹簧夹___________(填“a”或“b”),关闭另一个弹簧夹,抽拉注射器吸取250mL空气,再开、闭相应弹簧夹,缓缓推气体进入C装置,重复上述操作多次。当C中溶液颜色____________时,停止推动注射器的活塞;
④实验数据处理。
请回答下列问题:
(1)完善步骤③的内容________________;_____________。
(2)检查此装置气密性的操作是:_______________;
(3)该小组在同一地点进行了3组实验,推动活塞次数记录如下表(每次抽气为250mL)。进行3组实验的目的是_____________;综合3次实验数据分析:该测定地点的空气质量属于_________级标准
实验序号 | 推动次数 |
1 | 3 |
2 | 5 |
3 | 4 |
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某同学设计了测定空气中氧气含量的实验,实验装置如下图。
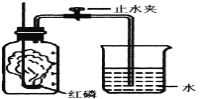
该同学的实验步骤如下:
①将图中的集气瓶分为5等份,并作好标记。
②在带橡皮塞和导管的燃烧匙内装入足量的红磷,将导管上的止水夹夹紧,在酒精灯上点燃红磷,并立即伸入集气瓶内,塞紧橡皮塞。
③充分反应后,待集气瓶冷却至室温,打开止水夹。
请回答下列问题:
(1)该实验中红磷需稍过量,目的是 。
(2)步骤③中打开止水夹后观察到的现象是 ,由此可得出空气中氧气的体积分数约为 。
(3)磷在空气中燃烧生成的氧化物通常可作强干燥剂。己知在标准状况下,32g氧气的体积是22.4L,在该条件下,制备71g这种干燥剂所消耗的空气的体积约为 L。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】一定条件下,氮的某种氧化物与NH3反应只生成N2和H2O。若生成N2和H2O的分子个数比为7:12,则该氮的氧化物的化学式为
A.N2O B.NO3 C.NO2 D.N2O5
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】请你参与兴趣小组的探究活动。
【提出问题】铁红中铁的质量分数是多少?(已知:工业铁红的主要成分是Fe2O3,还含有少量的FeO、Fe3O4。)
【查阅资料】
①草酸晶体(H2C2O4·3H2O)在浓H2SO4作用下受热分解,化学方程式为:
H2C2O4·3H2O![]() CO2↑+ CO↑+ 4H2O
CO2↑+ CO↑+ 4H2O
②浓H2SO4是液体,能有效吸收水分。
③碱石灰是氧化钙和氢氧化钠的混合物。
④一般来说,氢氧化钠溶液吸收二氧化碳的效果比氢氧化钙溶液好。
⑤铁的常见氧化物中铁的质量分数:
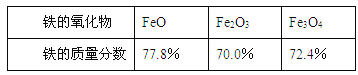
【实验与讨论】
(1)下列不能用作草酸分解制取气体的装置是 (填字母编号)。

(2)用下图所示装置进行实验,实验前应先 。
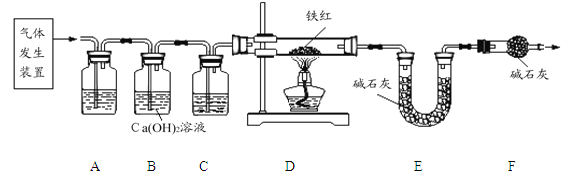
(3)进入D中的气体是纯净、干燥的CO,则A、C中的试剂依次是 、 (填字母编号)。
a.浓硫酸 b.澄清的石灰水 c.氢氧化钠溶液
(4)B装置的作用是 ,发生的化学方程式是
(5)写出D装置中含量最多的固体物质所发生反应的化学方程式 。
【数据分析与计算】
称取铁红样品20.0 g,用上述装置进行实验,测定铁红中铁的质量分数。
①D中充分反应后得到Fe粉的质量为m g,则 < m < 。
② 实验前后称得E装置增重13.2g,则此铁红中铁的质量分数是 。
【实验评价】
请指出图21-2中实验装置的一个明显缺陷 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com