

分析 (1)根据原子中质子数等于核外电子数,阴离子的核外电子数大于核内质子数,阳离子的核内质子数大于核外电子数分析解答;
(2)根据相对稳定结构的定义来分析;
(3)根据元素的种类由原子核内质子数所决定的,同种元素原子核内质子数相同;
(4)根据化学式的写法及化合物的构成微粒分析.
解答 解:
(1)阴离子的核外电子数大于核内质子数,所以属于阴离子的是:BDH;
(2)最外层为8个(只有一个电子层时为2个)为相对稳定结构,故达到相对稳定结构的粒子有 BDFG;其中F质子数等于核外电子数,是原子;
(3)元素的种类由原子核内质子数所决定的,上图共有7种元素;
(4)由微粒的结构示意图可知,E微粒可形成带二个单位正电荷的阳离子,由质子数是12可知为镁离子,而C微粒能形成带一个单位负电荷的阴离子,由质子数是9可知,为氟离子,因此形成稳定化合物的化学式为MgF2.
答案:
(1)BDH;
(2)F;
(3)7;
(4)MgF2.
点评 本题考查粒子结构示意图各部分的含义及化学式书写,质子数决定元素种类.


 永乾教育寒假作业快乐假期延边人民出版社系列答案
永乾教育寒假作业快乐假期延边人民出版社系列答案科目:初中化学 来源: 题型:选择题
| A. | H2 | B. | NH3 | C. | N2 | D. | N2O |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
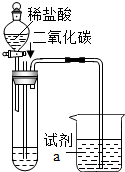 化学实验小组在做二氧化碳和氢氧化钠溶液反应的趣味实验.查阅资料如下:
化学实验小组在做二氧化碳和氢氧化钠溶液反应的趣味实验.查阅资料如下:| T/℃ | NaOH | Na2CO3 | NaCl |
| 20 | 109 | 21.8 | 36.0 |
| T/℃ | NaOH | Na2CO3 | NaCl |
| 20 | 17.3 | - | 0.1 |
| A. | ①②③④ | B. | ②③④⑤ | C. | ①②④⑤ | D. | ①②③⑤ |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 分子、原子都是不显电性的粒子,但不显电性的粒子不一定是分子或原子 | |
| B. | 燃烧都伴随着发光、放热,所以有发光、放热现象的就是燃烧 | |
| C. | 通常盐是由金属阳离子和酸根阴离子组成的,硝酸铵中没有金属阳离子,不属于盐 | |
| D. | 酸性溶液能使石蕊试液变红,滴入石蕊试液后变红的溶液一定是酸的溶液 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 次数 | 第一次 | 第二次 | 第三次 |
| 加入稀硫酸质量/g | 10 | 10 | 10 |
| 生成氢气质量/g | 0.04 | 0.04 | 0.02 |
查看答案和解析>>
科目:初中化学 来源: 题型:多选题
| A. | 3g碳在100g氧气中充分燃烧生成103g二氧化碳 | |
| B. | 100mL98%的浓硫酸用100mL水稀释,可得到溶质质量分数为49%的硫酸 | |
| C. | 用含杂质(杂质不与酸反应,也不溶于水)的铁10g 和50g 稀硫酸完全反应后,滤去杂质,所得液体质量为55.4g,则含杂质的铁中铁的质量分数为56% | |
| D. | MgO与CuO的混合物与98g10%的稀硫酸恰好完全反应,则原混合物中氧元素的质量是1.6g |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 科技日报北京2015年4月7日电美国华人科学家研制出首款可商业应用的高性能铝电池,其充电更快,寿命更长而且还很便宜,使用这种电池的智能手机充满电仅需一分钟.实验发现,用三维石墨作为电池正极材料,能极大缩短电池的充电时间.原理与铝空气电池相似,铝空气电池以高纯度铝Al(含铝99.99%)为负极、氧为正极,以氢氧化钾或氢氧化钠水溶液为电解质,铝摄取空气中的氧,在电池放电时产生化学反应,铝和氧作用转化为氧化铝.铅空气电池的进展十分迅速,是一种很有发展前途的空气电池.请回答有关间题:
科技日报北京2015年4月7日电美国华人科学家研制出首款可商业应用的高性能铝电池,其充电更快,寿命更长而且还很便宜,使用这种电池的智能手机充满电仅需一分钟.实验发现,用三维石墨作为电池正极材料,能极大缩短电池的充电时间.原理与铝空气电池相似,铝空气电池以高纯度铝Al(含铝99.99%)为负极、氧为正极,以氢氧化钾或氢氧化钠水溶液为电解质,铝摄取空气中的氧,在电池放电时产生化学反应,铝和氧作用转化为氧化铝.铅空气电池的进展十分迅速,是一种很有发展前途的空气电池.请回答有关间题:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com