
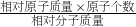 ×100%,进行分析判断.
×100%,进行分析判断.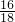 ×100%≈88.9%,则马来酸溶液的水中氧元素的质量分数为90%×88.9%=80%,进行分析判断.
×100%≈88.9%,则马来酸溶液的水中氧元素的质量分数为90%×88.9%=80%,进行分析判断.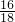 ×100%≈88.9%,马来酸溶液的水中氧元素的质量分数为90%×88.9%=80%,马来酸中还含有氧元素,故5%的马来酸溶液中氧元素的质量分数大于80%,故选项说法错误.
×100%≈88.9%,马来酸溶液的水中氧元素的质量分数为90%×88.9%=80%,马来酸中还含有氧元素,故5%的马来酸溶液中氧元素的质量分数大于80%,故选项说法错误.

科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
| A、马来酸属于氧化物 | B、马来酸中氧元素的质量分数最大 | C、马来酸中碳、氢、氧三种元素的质量比为1:1:1 | D、5%的马来酸溶液中氧元素的质量分数为2.76% |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com