
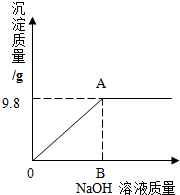
 有一包固体粉末,可能是CaCO3、Na2SO4、CuSO4、Na2CO3中的一种或多种,某实验小组对其组成成分进行了以下探究活动.
有一包固体粉末,可能是CaCO3、Na2SO4、CuSO4、Na2CO3中的一种或多种,某实验小组对其组成成分进行了以下探究活动.| 160 |
| y |
| 80 |
| x |
| 142 |
| z |
| 98 |
| 9.8g |
| 8g |
| 8% |
| 14.2+7.1 |
| 100+87.3-9.8 |
| 160 |
| y |
| 80 |
| x |
| 142 |
| z |
| 98 |
| 9.8g |
| 8g |
| 8% |
| 14.2+7.1 |
| 100+87.3-9.8 |


 Happy holiday欢乐假期暑假作业广东人民出版社系列答案
Happy holiday欢乐假期暑假作业广东人民出版社系列答案 快乐暑假暑假能力自测中西书局系列答案
快乐暑假暑假能力自测中西书局系列答案科目:初中化学 来源: 题型:

查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
| 实验装置 | 实验主要过程 |
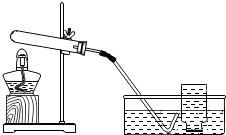 | ①检验装置气密性.操作如下:先将导管伸入液面下,用手紧握试管,观察到 ②加入过氧化钙,加热,导管口有大量气泡冒出. ③收集满一瓶气体.然后 ④停止加热.熄灭酒精灯前,应 ⑤检验气体.方法是 |
| 实验装置 | 实验主要过程 |
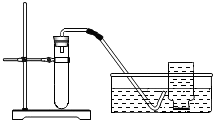 | ①检验装置气密性. ②加入过氧化钙和水后,有少量细小气泡缓慢放出,在导管口几乎收集不到气体.该装置放置到第二天,集气瓶只收集到极少量气体,振荡试管后仍有少量细小气泡缓慢放出. |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com