11、(1)①海水晒盐可得到粗盐和苦卤,其中苦卤是食盐的
饱和
(填“饱和”或“不饱和”)溶液,理由是
里面有析出的食盐晶体
.②利用苦卤.石灰乳.稀盐酸可制得应用于飞机制造业的金属镁.其中发生反应的化学方程式是①
MgCI2﹢Ca(OH)2=Mg(OH)2↓﹢CaCl2
;②
Mg(OH)2﹢2HCl=MgCl2﹢2H2O
;③
MgCl2=Mg﹢Cl2↑
.
(2)一包从海水中获得的粗盐,其中含有少量的泥沙等不溶性杂质,可采用以下步骤除去
溶解
.
过滤
.
蒸发
.课外活动小组对经过初步提纯的粗盐的成分进行探究,并将粗盐进一步提纯.
探究一:这包粗盐中还有什么杂质?
根据海水的成份和初步提纯的实验操作,估计粗盐中可能还有杂质是CaCl
2和MgCl
2,现用实验验证这种推测:①取样并溶解,加入数滴NaOH溶液,目的是检验有没有(化学式)
MgCl2
,相关的反应方程式为
MgCl2﹢2NaOH=Mg(OH)2↓﹢2NaCl
;②接着再加入数滴Na
2CO
3溶液,目的是检验其有没有(化学式)
CaCl2
,相关的反应方程式为
CaCl2+Na2CO3=CaCO3↓+2NaCl
.实验证明,这包粗盐中含有的杂质是CaCl
2.
探究二:这包粗盐中NaCl的质量分数是多少?
按下面步骤继续进行实验:①称取一定质量的样品;②将样品加水溶解制成粗盐溶液;③向粗盐溶液中加入过量某种试剂,过滤;④沉淀洗涤后小心烘干得到纯净固体A;⑤滤液在进行某一操作后,移入蒸发皿蒸发,得到纯净固体B;⑥称量实验中得到的某种固体.
②③⑤步骤中,都使用到同一仪器(填名称)
玻璃棒
,在步骤②和⑤中使用这种仪器采用了相同操作,但目的不同,在步骤②中的目的是
加速粗盐的溶解
,在步骤⑤中的目的是
防止由于局部温度过高,造成液滴飞溅
.步骤③中加入试剂是(化学式)
Na2CO3
,相关反应方程式为
CaCl2+Na2CO3=CaCO3↓+2NaCl
.步骤⑤进行的“某一操作”是
加入适量或过量的稀盐酸
,目的是
除去过量的碳酸钠
,相关反应方程式为
Na2CO3+2HCl=2NaCl﹢H2O﹢CO2↑
.步骤⑥中,你认为需要称量的固体是A还是B?
A
(填A或B)你不选择称量另一种固体的理由是
B中含有反应生成的氯化钠
.

 ×100%=4.75g,则氯化镁中氯元素的质量=4.75g-1.2g=3.55g
×100%=4.75g,则氯化镁中氯元素的质量=4.75g-1.2g=3.55g ×100%=5.55g,则氯化钙中氯元素的质量=5.55g-2g=3.55g
×100%=5.55g,则氯化钙中氯元素的质量=5.55g-2g=3.55g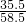 ×100%=58.5g
×100%=58.5g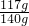 ×100%≈83.6%
×100%≈83.6%

 阅读快车系列答案
阅读快车系列答案
