
 (2007?宁夏)如图所示,在一只倒扣的大烧杯中,正放两只小烧杯.其中A杯中盛有足量浓盐酸,B杯中盛有少量滴有酚酞溶液的NaOH稀溶液.请回答:
(2007?宁夏)如图所示,在一只倒扣的大烧杯中,正放两只小烧杯.其中A杯中盛有足量浓盐酸,B杯中盛有少量滴有酚酞溶液的NaOH稀溶液.请回答:

科目:初中化学 来源: 题型:058
(2007
,宁夏回族自治区,15)如图所示,在一只倒扣的大烧杯中,正放两只小烧杯.其中A杯中盛有足量浓盐酸,B杯中盛有少量滴有酚酞溶液的NaOH稀溶液.请回答: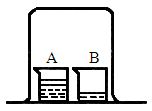
(1)
放置一段时间后,B杯中出现的现象是________.(2)
该现象说明浓盐酸具有的性质是________、________,写出有关反应的化学方程式:________.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com