
【题目】以下是初中化学的一些基本实验,其中不能达到相应的实验目的的是( )
A. 测定空气中O2的含量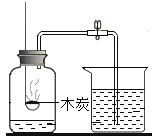
B. 稀释浓硫酸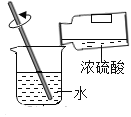
C. 铁丝在空气中的变化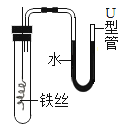
D. 一氧化碳还原氧化铁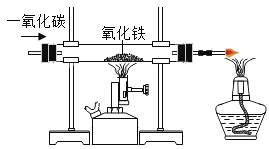
 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:
【题目】实验室现有如下实验用品:高锰酸钾、稀盐酸、石灰石、火柴、药匙、镊子、升降台及以下仪器。请回答下列问题,并按要求填写相关空白:
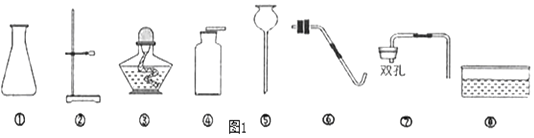
(1)若补充仪器______(填名称)和用品______,并利用上述部分仪器和药品可制取一种气体,则发生反应的化学方程式______。
(2)如图是实验室制备、干燥和收集二氧化碳气体的装置图,按照上述顺序,仪器连接顺序为a应该连______(填“c”或“d”)。装置C中装的液体为______,画出装置C中的液体示意图。
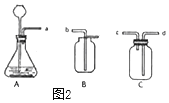
(3)用B装置收集二氧化碳的原理是:二氧化碳气体______,二氧化碳气体向集气瓶的______部运动,随着瓶内气体的增多,______,在压强差的作用下,瓶内空气向______运动被排出集气瓶,瓶内剩余气体为二氧化碳气体。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】人类的日常生活和工农业生产离不开水。请回答:
(1)含有较多可溶性钙、镁化合物的水叫做______________(填“软水”或“硬水”)。
(2)软化生活用水常用的方法是__________________。
(3)下列净化水的单一操作中,相对净化程度较高的是_____________(填字母)
A.静置沉淀 B.吸附沉淀 C.蒸馏
(4)水通电可以分解,其反应的化学方程式_______________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】H7N9型禽流感是一种新型禽流感,至今尚未有疫苗推出.达菲(C16H28N2O4H3PO4)可用于H7N9的前期抗病毒治疗.生产达菲的主要原料﹣﹣莽草酸(C7H10O5)可从我国盛产的八角茴香中提取.可用以下方法从八角茴香中提取莽草酸:1、将粉碎的八角茴香用有机溶剂脱脂;2、用有机溶剂浸泡脱脂物料;3、过滤;4、用活性炭脱色;5、经真空减压蒸发浓缩后再过滤,得粗晶体.
(1)从八角茴香中提取莽草酸的过程中,用活性炭脱色是利用了活性炭的_____性;需经真空减压蒸发浓缩而不能直接在空气中加热蒸发,主要是为了防止加热时莽草酸被氧化,试写出莽草酸在空气中燃烧的化学方程式:_____
(2)给病人注射用的注射器由不锈钢制的针头和塑料制的针筒两部分组成.其中,塑料属于_____材料;医院里常用高温蒸煮的方法给医疗器械消毒,其原理是_____.
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某化学小组利用如图所示装置(图中固定装置已略去)测定铜锌合金中锌的质量分数,探究过程如下:
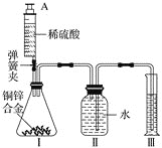
①连接实验装置并检查装置气密性。
②向装置Ⅰ中的锥形瓶加入2.0g的铜锌合金样品粉末,由注射器缓缓注入稀硫酸,待到锥形瓶中不再产生气体时,准确读取注射器内读数,减少10.5mL稀硫酸,同时立即夹紧弹簧夹,移出装置Ⅲ中的导管,准确读取量筒内水的体积为214.0mL(注:样品中的杂质不参加反应
③装置Ⅰ中剩余固体物质经过适当处理后,准确称量其质量为1.4g
④该小组的三位同学利用实验过程测得不同数据,计算铜锌合金样品中锌的质量分数
甲同学利用装置Ⅰ中反应前后固体的质量进行计算;
乙同学利用装置Ⅰ中加入稀硫酸的量进行计算;
丙同学利用装置Ⅲ中量取水的体积进行计算,并查得:在标准状况下,氢气的密度为0.09gL-1。
回答下列问题:
(1)装置Ⅰ中反应的化学方程式为___,实验过程中须加入稀硫酸至不再产生气体,目的是___。
(2)步骤③中称量剩余固体之前的正确操作是_______、洗涤、干燥。
(3)根据实验测定的数据,上述三位同学中________(填“甲”、“乙”或“丙”)同学无法进行计算样品中锌的质量分数。
(4)化学小组同学发现:按照丙同学的方案进行计算,致使实验结果出现较大偏差。以下因素可能造成偏差的有________(填标号)。
A 移出装置Ⅲ时,导管内留存了一部分水
B 实验测量前,没有排除装置Ⅰ中的空气
C 数据处理时,未排除加入稀硫酸所占的体积
【答案】(1)![]() ;使样品中的锌完全反应;(2)过滤;(3)乙;(4)AC;
;使样品中的锌完全反应;(2)过滤;(3)乙;(4)AC;
【解析】
试题(1)由于铜排在了氢的后面,所以与酸不反应,反应物是锌和硫酸,生成物是硫酸锌和氢气,氢气后面标上上升符号;实验过程中须加入稀硫酸至不再产生气体,目的是使样品中的锌完全反应;(2)从铜和硫酸锌溶液的混合物中得到铜,先进行过滤,得到带有硫酸锌溶液的铜,再进行洗涤除去表面的硫酸锌,再进行干燥除去水即可;(3)根据加入稀硫酸的量进行计算需要知道稀硫酸的溶质质量分数,而题中没有告知;(4)由于锌与硫酸反应生成硫酸锌和氢气时,放出热量,如果没等冷却到室温,根据热涨冷缩的原理可知进入量筒中水偏多,所以误认为得到的氢气多,再就是数据处理时,未排除加入稀硫酸所占的体积,计算的结果就偏大;
考点:金属的化学性质;化学方程式;实验误差分析;
点评:熟记金属活动性顺序表,知道排在氢之前的金属和稀盐酸或者硫酸反应生成氢气,而排中氢之后的金属和稀盐酸或者稀硫酸不生成氢气;化学反应中物质的质量比都是纯净物之间的质量比,而溶液中溶质的质量=溶液质量×溶质质量分数;本题容易出错的地方是对实验结果的评价,要知道锌与硫酸反应放出热量,会造成相应的误差,必须冷却到室温才能进行观察和计算。
【题型】实验题
【结束】
30
【题目】用1000t含氧化铁80%的赤铁矿石,理论上可以炼出含铁96%的生铁的质量是多少?
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某纯碱样品中含有少量NaCl,小丽同学取该样品23g全部溶解于150g水中,再逐滴加入160g稀盐酸,反应中产生的气体的质量与盐酸的用量关系如图所示。(提示:相关反应为Na2CO3+2HCl=2NaCl+H2O+CO2↑)计算当恰好完全反应时:
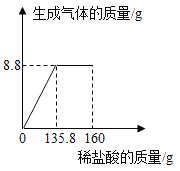
(1)产生的二氧化碳的质量是 克。
(2)此时所得到的溶液中溶质的质量分数(写出必要的计算过程,结果保留到0.1%)。
查看答案和解析>>
科目:初中化学 来源: 题型:
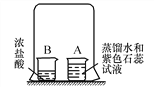
【题目】在烧杯A中装入20 mL蒸馏水,滴入2~3滴紫色石蕊试液;在烧杯B中装入10 mL浓盐酸,然后用一只大烧杯把A、B两烧杯罩在一起(如图所示)。过几分钟后,可以观察到烧杯A中液体变成________色。由该实验可知(浓)盐酸具有的性质是:
(1)_____________________________________________________________;
(2)____________________________________________________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】水是人类宝贵的自然资源,与人类的生产、生活密切相关。
(1)水是常见的溶剂,将下列生活中少量的物质分别放入水中,不能形成溶液的是__________。
A 食盐B 面粉C 植物油D 蔗糖
(2)电解水时,正、负极产生气体的体积比是__________。发生反应的化学方程式为_______ 。
(3)天然水中含有许多杂质,净化水的方法有:①过滤 ②蒸馏③加明矾吸附沉降④消毒杀菌⑤活性炭层吸附。要把天然水净化成生活用的自来水,将所选用的净化方法按净化过程排序是______(填序号)。
(4)区别净化后的自来水是硬水还是软水,可用到的物质是___________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】亚硫酸钠是种常见食品添加剂,亚硫酸钠在加热条件下可以和酸反应生成氧化硫气体。为检验某食品中亚硫酸钠的含量(以1kg样品生成的SO2质量计),某研究小组设计了如下实验流程:

(1)为防止煮沸时发生暴沸,可以先向烧瓶中加入___________________________.在实验装置中先通入![]() 的目的是___________________________.
的目的是___________________________.
(2)写出氢氧化钠溶液吸收SO2的化学方程式:_______________________________________________.
(3)要得到SO2的质量,实验中需要称量反应前碱液的质量和_____________的质量。
(4)若用盐酸代替稀硫酸处理样品,则对实验结果的影响是_____________(填“偏高”、“偏低”或“无影响”),这是因为盐酸具有_____________性。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com