
| A. | 实验说明:同种物质的溶液浓度大小不同时,化学性质可能不同 | |
| B. | 实验中除了生成SO2,还会生成CO2 | |
| C. | 实验中生成SO2的质量等于3.2g | |
| D. | 用此反应制取ZnSO4与用锌与稀硫酸相比,不仅有污染,而且不经济 |
分析 A、根据浓硫酸和稀硫酸的性质分析;
B、根据浓硫酸在反应过程中会逐渐稀疏成稀硫酸分析;
C、据浓硫酸在反应过程中会逐渐稀疏成稀硫酸,浓稀硫酸与锌反应的产物不一样判断;
D、根据锌和稀硫酸、锌和浓硫酸反应的化学方程式比较判断.
解答 解:A、因为锌和稀硫酸反应生成氢气,锌和浓硫酸反应生成二氧化硫,所以同种物质的溶液浓度大小不同时化学性质,故A正确;
B、在反应过程中浓硫酸的浓度逐渐降低变成稀硫酸,稀硫酸和锌反应生成氢气,所以还会生成氢气,故B错误;
C、10g98%的浓硫酸含有硫酸9.8g,根据化学方程式理论上产生3.2g二氧化硫,但浓硫酸的浓度逐渐降低变成稀硫酸
稀硫酸和锌反应生成氢气,而不生成二氧化硫,故C错误;
D、由Zn+H2SO4(稀)═ZnSO4++H2↑知,锌和硫酸反应微粒个数比是1:1,而在Zn+2H2SO4(浓)═ZnSO4+SO2↑+2H2O反应中,锌和硫酸反应微粒个数比是1:2,所以用锌与浓硫酸反应制ZnSO4除了污染大,还有消耗硫酸的量大,故D错误.
故选:AD.
点评 本题通过稀硫酸和浓硫酸化学性质不同,反应的产物不同,让我知道物质的浓度不仅能改变反应的速率,还能改变物质的性质.


 习题精选系列答案
习题精选系列答案科目:初中化学 来源: 题型:实验探究题
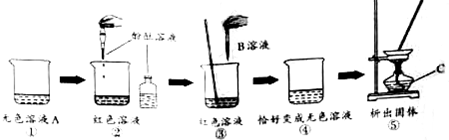
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 进入山洞前要做灯火实验,因为二氧化碳有毒会致人死亡 | |
| B. | 用过量的稀盐酸长时间浸泡除去铁锅中的水垢(主要成分为碳酸钙) | |
| C. | 市场上有“葡萄糖酸锌”、“加碘食盐”等商品,这里的碘、锌是指元素 | |
| D. | 厨房内天然气泄露时,立即打开排气扇 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
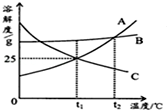
| A. | t1℃时,A的饱和溶液中溶质质量分数为20% | |
| B. | t2℃时A、B、C的溶解度大小为A=B>C | |
| C. | t2℃时等质量的饱和溶液中溶剂质量:C>A=B | |
| D. | t2℃A、B、C的饱和溶液降温到t1℃时,A、C两溶液中溶质的质量分数相等 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题

查看答案和解析>>
科目:初中化学 来源: 题型:填空题
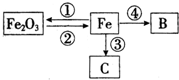 构建知识网络是一种重要的学习方法.图是关于铁化学性质的知识网络,其中B是密度最小的气体,C为红色固体单质.请回答下列问题:
构建知识网络是一种重要的学习方法.图是关于铁化学性质的知识网络,其中B是密度最小的气体,C为红色固体单质.请回答下列问题:查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com