

���� ϡ������������Ʒ�Ӧ���������ƺ�ˮ������ͭ���������Ʒ�Ӧ����������ͭ��ɫ�����������ƣ����ݷ�Ӧ�Ļ�ѧ����ʽ�����ṩ�����ݿ��Խ�����ط���ļ�����жϣ�
��� �⣺��1������ͭ���������Ʒ�Ӧ����������ͭ��ɫ�����������ƣ���Ӧ�Ļ�ѧ����ʽΪ��2NaOH+CuSO4=Cu��OH��2��+Na2SO4��
���2NaOH+CuSO4=Cu��OH��2��+Na2SO4��
��2��������ͭ������Ϊx��
2NaOH+CuSO4=Cu��OH��2��+Na2SO4��
160 98
x 4.9g
$\frac{160}{98}$=$\frac{x}{4.9g}$��
x=8g��
���$\frac{160}{98}$=$\frac{x}{4.9g}$��
��3��������ͭ�����������Ƶ�����Ϊy��
2NaOH+CuSO4=Cu��OH��2��+Na2SO4��
80 98
y 4.9g
$\frac{80}{98}$=$\frac{y}{4.9g}$��
y=4g��
����������Ϊz��
�����ᷴӦ��������������Ϊ��120g��10%-4g=8g��
2NaOH+H2SO4�TNa2SO4+2H2O��
80 98
8g z
$\frac{80}{98}$=$\frac{8g}{z}$��
z=9.8g��
��һ��ʵ����������������Һ��������������Ϊ��40g��10%=4g����˵�һ��ʵ���������������������Һ�������з�Ӧ���ɵ������ơ�û�з�Ӧ������ͭ�����ᣬ��ѧʽ�ֱ���Na2SO4��CuSO4��H2SO4��
���Na2SO4��CuSO4��H2SO4��
��4���û����Һ�����������ͭ��������Ϊ��9.8g��8g=49��40��
���49��40��
��5����2NaOH+CuSO4=Cu��OH��2��+Na2SO4��2NaOH+H2SO4�TNa2SO4+2H2O��֪��2NaOH��Na2SO4��
�跴Ӧ��������������Ϊm��
2NaOH��Na2SO4��
80 142
120g��10% m
$\frac{80}{142}$=$\frac{120g��10%}{m}$��
m=21.3g��
����˺�������Һ�м���84.9gˮ��������Һ�����ʵ���������Ϊ��$\frac{21.3g}{100g+120g+84.9g-4.9g}$��100%=7.1%��
���7.1%��
7.1%��
���� ������Ҫ����ѧ�����ü��跨�ͻ�ѧ����ʽ���м�����ƶϵ�����������ʱҪע��淶�Ժ�ȷ�ԣ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| ѡ�� | ���ֵ����� | ���ַ��� |
| A | �ڴͽ��� | ������ζ �ڳ�ζ�� |
| B | ʳ�κ���Na2CO3�� | �ټ�ʳ�� ������ͷ |
| C | �ƽ�ͻ�ͭ���ٻƽ� | ������ �ڲ��ܶ� |
| D | ����ˮ������ˮ | ������ �ڿ���ɫ |
| A�� | A | B�� | B | C�� | C | D�� | D |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 9.1% | B�� | 11.8% | C�� | 13.3% | D�� | 15.3% |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��ƶ���
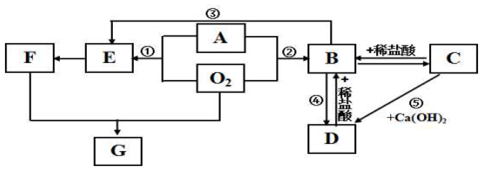
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ������˿���Ż�� | B�� | ������˿���¶� | ||
| C�� | ���ӿ�ȼ�� | D�� | �����������ĽӴ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ��̽����
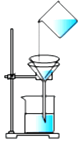 ijͬѧ�����ǵĺ�ˮ��Ʒ�����ձ��У��ȼ������������ܽ⣬����һ���������ͼ��ʾ�����ʣ�
ijͬѧ�����ǵĺ�ˮ��Ʒ�����ձ��У��ȼ������������ܽ⣬����һ���������ͼ��ʾ�����ʣ��鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��ƶ���
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com