
【题目】已知两种活动性不同的金属在能导电的溶液中接触可以形成原电池,从而加快化学反应速率.在实验室里,我们常用锌与稀硫酸反应来制取氢气(装置如图所示). 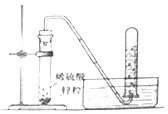
(1)实验室用锌与稀硫酸反应制取氢气的化学方程式为 .
(2)实验室也可用锌与盐酸反应来制取氢气,但制得的氢气中往往含有HCl气体,若将制得的气体通过盛有NaOH溶液的洗气瓶,(填“能”或“不能”)得到纯净的氢气.
(3)点燃氢气之前,先要进行的操作是 .
(4)锌与稀硫酸反应时,加入某些盐溶液可使制取H2的速率加快,如溶液.
(5)图示装置,(填“能”或“不能”,药品可换)用来制取CO2气体.
【答案】
(1)Zn+H2SO4=ZnSO4+H2↑
(2)不能
(3)检验氢气的纯度
(4)硫酸铜(答案合理即可)
(5)不能
【解析】解:(1)锌和硫酸反应生成硫酸锌和氢气,化学方程式为:Zn+H2SO4=ZnSO4+H2↑;故填:Zn+H2SO4=ZnSO4+H2↑;(2)氢氧化钠溶液可以吸收氢气中混有的氯化氢气体,但是氢气通过溶液中又会带出水蒸气,不能得到纯净的氢气;故填:不能;(3)可燃性气体与空气混合后点燃可能发生爆炸,为防止发生爆炸,点燃可燃性气体之前必须检验气体的纯度.故填:检验氢气的纯度;(4)两种活动性不同的金属在能导电的溶液中接触可以形成原电池,从而加快化学反应速率,所以加入硫酸铜溶液,锌能置换出硫酸铜中的铜,铜与锌在稀硫酸中形成原电池,使制取H2的速率加快,故填:硫酸铜(答案合理即可);(5)二氧化碳能溶于水,所以不能用排水法来收集二氧化碳,故填:不能.
【考点精析】解答此题的关键在于理解氢气的制取和检验的相关知识,掌握氢气的实验室制法原理:Zn + H2SO4 = ZnSO4 +H2↑;Zn + 2HCl = ZnCl2 +H2↑不可用浓盐酸的原因 浓盐酸有强挥发性 ;不可用浓硫酸或硝酸的原因 浓硫酸和硝酸有强氧化性,以及对书写化学方程式、文字表达式、电离方程式的理解,了解注意:a、配平 b、条件 c、箭号.


科目:初中化学 来源: 题型:
【题目】粗盐中MgCl2、CaCl2等杂质,提纯粗盐的工艺流程如图所示.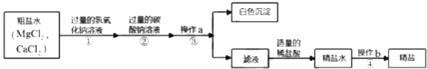
回答下列问题:
(1)氢氧化钠有强烈的腐蚀性,如果不慎沾到皮肤上,要用大量的水冲洗,再涂上;
(2)步骤②加入过量的碳酸钠溶液的作用是;
(3)操作a的名称是;
(4)步骤④中,要用玻璃棒不断搅拌,其目的是 .
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】用熟石灰中和一定量的盐酸时,溶液的pH与加入的熟石灰质量的关系如右图所示。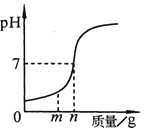
熟石灰与盐酸反应的化学方程式为;当加入熟石灰mg时,溶液中的溶质为 。若改用n g氢氧化钠与相同量盐酸反应,所得溶液的pH7(填“>”、“<”或“=”)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】化学试剂厂三个车间排放的废液中分别含有的溶质如下:
甲 | 乙 | 丙 |
Ba(OH)2、NaOH | NaCl、Na2CO3 | HCl、NaCl |
按照不同的方式处理,可以得到不同化学产品,从而充分利用资源,变废为宝.
(1)方案一,甲车间废液中加入适量的Na2CO3 溶液,可分离回收Ba(OH )2 和 NaOH,写出该反应的化学方程式;
(2)方案二,乙、丙两车间的废液按适当比例混合后,可得到一种溶质为的中性溶液;
(3)方案三,将三个车间的废液样品混合,过滤.得到无色溶液和白色沉淀.无色溶液中一定含有NaCl,为确定可能含有的溶质,设计下列实验,其中能达到目的是
A.若只加入MgSO4 溶液,能观察到明显现象
B.若加入过量的Na2CO3 溶液后,再滴加石蕊溶液,都能观察到明显现象
C.若加入过量的中性BaCl2 溶液后,再滴加酚酞溶液,都能观察到明显现象
(4)方案四,按照下列方式将三个车间的废液按适当比例混合(假设能反应的物质均恰好完全反应,且中间过程未过滤),最终只生成BaCO3 沉淀和NaCl 溶液的是 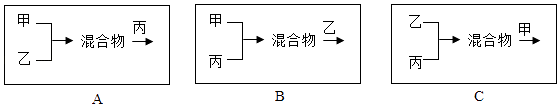
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列反应中属于化合反应的是( )
A.2Na+2H2O═2NaOH+H2↑
B.Fe2(SO4)3+Fe=3FeSO4
C.CaCO3 ![]() CaO+CO2↑
CaO+CO2↑
D.2NaCl+2H2O ![]() 2NaOH+Cl2↑+H2↑
2NaOH+Cl2↑+H2↑
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】我国在2017年“世界环境日”(6月5日)确定的主题是“绿水青山,就是金山银山”.华雪与同学们积极参加了这一主题的活动,在老师的指导下,他们对一造纸厂排放的污水进行检测,发现其主要的污染物为NaOH.为了测定污水中NaOH的含量,他们首先把溶质质量分数为98%(密度1.84g/cm3)的浓硫酸20g,稀释为质量分数为10%的硫酸;然后取80g污水于烧杯中,逐滴加入10%的硫酸至49g时恰好完全反应(假定污水中的其它成分不与硫酸反应).请计算:
(1)把20g上述浓硫酸稀释为质量分数为10%的硫酸,需要水的质量是g.
(2)污水中所含NaOH的质量分数是多少?(写出计算过程)
(3)取80g该污水于烧杯中放置几天后,若其中的氢氧化钠全部转化为碳酸钠.则此时应逐滴加入10%的硫酸克才能使碳酸钠恰好完全变成硫酸钠.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com