
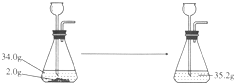
 实验室用硫酸铜作过氧化氢溶液制取氧气的催化剂.现在2.0g硫酸铜中加入34.0g过氧化氢溶液,充分反应后液体的总质量为35.2g.试计算:
实验室用硫酸铜作过氧化氢溶液制取氧气的催化剂.现在2.0g硫酸铜中加入34.0g过氧化氢溶液,充分反应后液体的总质量为35.2g.试计算:分析 (1)利用催化剂的有关性质分析解答即可;依据氧气的质量利用方程式即可求出过氧化氢的质量,进而得到过氧化氢溶液中溶质质量分数;
(3)剩余的溶液中溶质即为硫酸铜,利用溶液的质量即可求出剩余溶液中溶质的质量分数;
解答 解:(1)由于硫酸铜是该反应的催化剂,所以化学反应前后其质量不会变化,故反应后硫酸铜的质量为2.0g,由质量守恒定律可知生成氧气的质量是34.0g+2.0g-35.2g=0.8g
(2)设该过氧化氢的溶质质量为x
2H2O2$\frac{\underline{\;CuSO_{4}\;}}{\;}$2H2O+O2↑
68 32
x 0.8g
$\frac{68}{x}=\frac{32}{0.8g}$
x=1.7g
过氧化氢溶液的溶质质量分数=$\frac{1.7g}{34g}×$100%=5%
(2)反应后所得硫酸铜溶液的溶质质量分数为:
$\frac{2g}{35.2g}×$100%=5.7%
答案:
(1)过氧化氢溶液的溶质质量分数为5%
(2)反应后所得硫酸铜溶液的溶质质量分数为5.7%.
点评 本题主要考查学生运用化学方程式和溶质质量分数公式进行计算的能力及考查学生运用质量守恒定律和化学方程式以及质量分数公式进行计算的能力.


科目:初中化学 来源: 题型:解答题



| 阴离子 阳离子 | OH- | CO32- |
| Ca2+ | 微 | 不 |
| Mg2+ | 不 | 微 |
| 实验步骤 | 实验现象 | 实验结论 |
| 步骤一:取一定量的氯化钠溶液于试管中,加入适量的NaOH溶液 | 无明显现象 | 说明MgCl2已(填“已”或“未”)除尽 |
| 步骤二:往步骤一所得溶液中加入适量的Na2CO3 溶液 | 产生白色沉淀 | 说明溶液中含有CaCl2 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | Mg和稀硫酸 | B. | MgCO3和稀硫酸 | ||
| C. | Mg和CuSO4溶液 | D. | MgCl2溶液和Na2SO4溶液 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com