解:(1)铁丝燃烧生成四氧化三铁,化学方程式为:3Fe+2O
2
Fe
3O
4.
(2)铁的常见氧化物有三种:Fe
2O
3、FeO、Fe
3O
4;
(3)氢氧化钠与硫酸亚铁反应的生成物是氢氧化亚铁与硫酸钠,因为氢氧化亚铁属于另一反应的反应物了,所以副产品是硫酸钠;冷却热饱和溶液 的过程是先加热,再降温,析出晶体后过滤再通过加热除去结晶水即可;
(4)通过反应Fe(OH)
2+2Fe(OH)
3
Fe
3O
4+4H
2O可知Fe(OH)
2和Fe(OH)
3都是反应物,如果不控制“一定量空气”氧气过多会把氢氧化亚铁全部氧化,就得不到四氧化三铁了;
故答案为:(1)3Fe+2O
2
Fe
3O
4.(2)Fe
2O
3或FeO.(3)Na
2SO
4 c→a(4)控制Fe(OH)
2的转化量(或答防止Fe(OH)
2全部转化为Fe(OH)
3)
分析:(1)根据反应物生成物及反应条件写出化学方程式
(2)根据铁的化合价写出氧化物化学式;
(3)根据氢氧化钠与硫酸亚铁反应的生成物来判断副产品,根据冷却热饱和溶液的过程考虑操作顺序;
(4)如果氧气过多会把氢氧化亚铁全部氧化,就得不到四氧化三铁了
点评:通过回答本题知道了制取四氧化三铁的方法,由溶液析出晶体的方法.


 Fe3O4+4H2O.生产流程中控制“一定量空气”的目的是______.
Fe3O4+4H2O.生产流程中控制“一定量空气”的目的是______. Fe3O4.
Fe3O4. Fe3O4+4H2O可知Fe(OH)2和Fe(OH)3都是反应物,如果不控制“一定量空气”氧气过多会把氢氧化亚铁全部氧化,就得不到四氧化三铁了;
Fe3O4+4H2O可知Fe(OH)2和Fe(OH)3都是反应物,如果不控制“一定量空气”氧气过多会把氢氧化亚铁全部氧化,就得不到四氧化三铁了; Fe3O4.(2)Fe2O3或FeO.(3)Na2SO4 c→a(4)控制Fe(OH)2的转化量(或答防止Fe(OH)2全部转化为Fe(OH)3)
Fe3O4.(2)Fe2O3或FeO.(3)Na2SO4 c→a(4)控制Fe(OH)2的转化量(或答防止Fe(OH)2全部转化为Fe(OH)3)

 开心快乐假期作业暑假作业西安出版社系列答案
开心快乐假期作业暑假作业西安出版社系列答案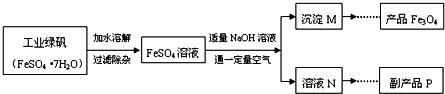

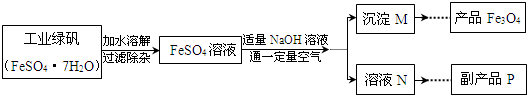
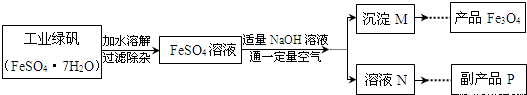
 Fe3O4+4H2O.生产流程中控制“一定量空气”的目的是 .
Fe3O4+4H2O.生产流程中控制“一定量空气”的目的是 .