
| A. | 0个 | B. | l个 | C. | 2个 | D. | 3个 |
分析 在金属活动性顺序中只要排在前面的金属就能把排在后面的金属从其盐溶液中置换出来;用同种金属置换不同的盐溶液,盐中金属排在金属活动性顺序中较后的金属首先被置换出来.用不同的金属置换同种盐溶液,盐中金属先被排在金属活动性顺序中较前的金属置换出来.另外,若有一种金属和多种混合盐溶液反应,最先反应的是最不活泼的那个金属的盐溶液.可以据此分析该题.
解答 解:由金属活动性顺序表可知,Mg>Fe>Ag,向AgNO3溶液中加入一定质量Mg和Fe的混合粉末,镁首先与硝酸银溶液反应,当镁反应完后,铁与与硝酸银溶液反应,由得到滤渣和浅绿色滤液,说明了溶液中含有硝酸亚铁,说明了镁已完全反应,滤渣中一定含有银,由以上分析可知:
①由于没有提及具体的镁和铁的量,所以不能判断金属铁是否剩余,而银不能和酸反应,所以不能判断一定产生气泡,故①错;
②由于没有提及具体的镁和铁的量,所以不能判断是否将硝酸银全部置换出来,所以不能判断一定产生沉淀,故②错;
③由于镁和铝的活动性都比银强,所以在滤渣中一定含有银单质,结合滤液颜色是浅绿色,说明镁完全反应,铁参加反应,因此一定没有镁,可能含有铁,故③对;
④溶液得到是浅绿色溶液,所以可以判断镁已完全反应,所以在滤液中一定含有硝酸镁和硝酸亚铁,可能含有硝酸银,故④错;
即题中所给的说法正确的只有③,即只有一种说法正确.
故选B.
点评 解答这类题目时,首先,要熟记和理解金属活动性顺序及其应用,以及与之相关的知识等;然后,根据所给问题情景结合所学的相关知识和技能,细致地阅读、分析题意等细心地进行探究、推理,最后,按照题目的要求,认真地进行选择或解答即可.


科目:初中化学 来源: 题型:解答题
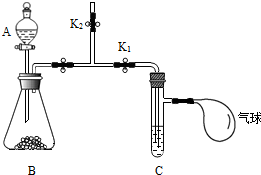 某化学兴趣小组利用如下装置探究两个实验.
某化学兴趣小组利用如下装置探究两个实验.查看答案和解析>>
科目:初中化学 来源: 题型:解答题
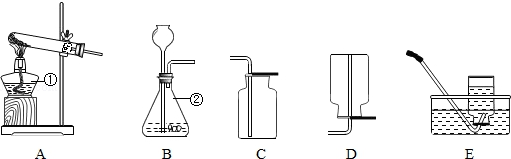
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | ①② | B. | ①③ | C. | ②④ | D. | ①④ |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
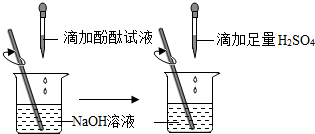
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
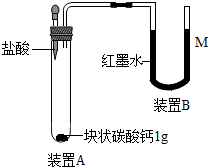 小军设计如图装置进行制取CO2的实验探究,经检验该装置气密性良好.
小军设计如图装置进行制取CO2的实验探究,经检验该装置气密性良好.查看答案和解析>>
科目:初中化学 来源: 题型:多选题
| A. | 水烧开后易把壶盖冲起--说明温度升高分子会变大 | |
| B. | 公园的桂花开放时满园飘香--说明分子在不断运动 | |
| C. | 液氧和氧气状态不同,但化学性质相同--它们都由氧分子构成 | |
| D. | 喝了汽水后,常常会打嗝--气体的溶解度随压强的减小而减小 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com