
| ������ | Fe��OH��2 | Fe��OH��3 | Cu��OH��2 | Mn��OH��2 |
| ��ʼ���� | 7.5 | 2.7 | 5.2 | 8.3 |
| ��ȫ���� | 9.7 | 3.2 | 6.4 | 9.8 |
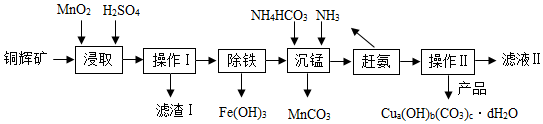
���� ���ݸ�����ת����ϵ��Ӧ�Ĺ��̷���ÿ����Ӧ�����⣬����ֱ�ӷ���ÿ�����⣬�Ӹ�������Ϣ���Ҷ�Ӧ����Ϣ��
��� �⣺
��1������I�����Ľ���ǵõ����������Ըò���Ϊ���ˣ�������II�����Ľ���õ���Һ�����Ըò���Ҳ�ǹ��ˣ��ڹ��˲����в�������������������
��2������ȡ�������з�����Ӧ��I��II�������з�ӦIΪ��2MnO2+Cu2S+��H2SO4=2MnSO4+2CuSO4+S��+4H2O���������ɵ�ˮ�е���ԭ�Ӷ��������ᣬ������ԭ�Ӹ�����֪����ļ�����Ϊ4�����С������Ϻ��ʵĻ�ѧ������Ϊ 4��
��3������ȡ�������У����ڴ����������������������ᷴӦ������������ˮ����Ӧ�Ļ�ѧ����ʽΪ Fe2O3+3H2SO4=Fe2��SO4��3+3H2O��
��4������I�ijɷ�ΪMnO2��S�����ɵģ���SiO2��ͭ�Կ��еģ������ʣ�
��5��
| ������ | Fe��OH��2 | Fe��OH��3 | Cu��OH��2 | Mn��OH��2 |
| ��ʼ���� | 7.5 | 2.7 | 5.2 | 8.3 |
| ��ȫ���� | 9.7 | 3.2 | 6.4 | 9.8 |
���� ��ͼ�����л�ý����Ŀ�������Ϣ�������ڽ����Ŀʱ�ȿ�����������ʲô��Ȼ���������ȥ��������ͼ����ȥѰ�ҽ�����õ���Ϣ�������������Ϣ������Ч�ԣ���������ʵ�����븴�ӵ�ת��ͼ��ȣ���ʵ�ܼܻ��������߿���˵ת��ͼ�ṩ�����龳���������֪ʶ��


 ������ÿ�ʱ��ҵϵ�д�
������ÿ�ʱ��ҵϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ��ƶ���

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�����ӵķ��� | B����ѧ�����еġ����� |
| ��ȥCO�е�CO2--ͨ��NaOH��Һ ľ̿���л�������--�ô������� ��ȥ�����е�����--ͨ�����ȵ�ͭ�� | ����ʯȼ��--ú����Ȼ����ʯ�� ���ֺ�ɫ������--CuO��MnO2��Fe3O4 ϡ����Һ��������--���㡢��ȡ������ |
| C���ճ����ʵ����� | D��ʵ�鰲ȫע������ |
| Ӳˮ����ˮ--�ӷ���ˮ������ ���ͺ�ʳ��--����ζ ��Ƭ��Ƭ--��̻����Ƚ�Ӳ�� | ��ȡ����--�ȼ��װ�õ������� ������Ȼ��й©--Ҫ���������� ���Ż�--��ˮ���� |
| A�� | A | B�� | B | C�� | C | D�� | D |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
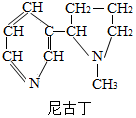 ��ͼΪ�������к�������Ŷ��Ľṹʽ�����ߴ������Ӷԣ���������ʵĻ�ѧʽΪC10H14N2�������ʵ���Է�������Ϊ162��
��ͼΪ�������к�������Ŷ��Ľṹʽ�����ߴ������Ӷԣ���������ʵĻ�ѧʽΪC10H14N2�������ʵ���Է�������Ϊ162���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| ����������� | ���� | |
| A | NaOH��NaCl��HCl������Һ | ������ɫʯ����Һ������ɫ |
| B | �ƽ�ͼٻƽ�ͭп�Ͻ� | �μ�ϡ���ᣬ���Ƿ������ݲ��� |
| C | �ռ�ʹ��� | �μӳ���ʯ��ˮ�����Ƿ������ɫ���� |
| D | Ӳˮ����ˮ | �۲��Ƿ���� |
| A�� | A | B�� | B | C�� | C | D�� | D |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
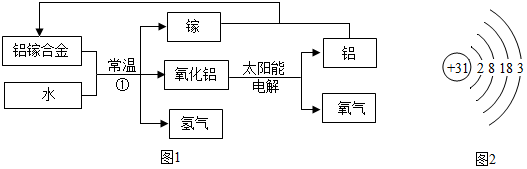
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �����Ͻ��Ʒɻ����������Ӳ�ȴ��ܶ�С����ʴ | |
| B�� | ���������õ�Һ�⡢Һ����������Ⱦ�Ĵ����� | |
| C�� | ϡ������ͨ��ʱ�ᷢ��������ɫ�Ĺ⣬���õ�����ѧ�����ȶ� | |
| D�� | �����г��ü�����еķ�������ˮ��Ӳ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ��̽����

�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com